
Jaime S, #MEAction, 14 januari 2019
Hoewel audio een beetje te snel gaat om de wetenschappelijke details te snappen, kan je het artikel ook beluisteren op Soundcloud van #MEAction [in het Engels].
We zijn verheugd en trots om aan te kondigen dat onze twee onderzoeksfellows, Sydney A. Brumfield en Paula S. Lara Mejia, hun eerste professionele wetenschappelijke artikel over myalgische encefalomyelitis geschreven en uitgegeven hebben in samenwerking met hun mentor Michael B. VanElzakker. Het artikel, Neuroinflammation and Cytokines in Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): A Critical Review of Research Methods [Neuro-inflammatie en cytokines bij Myalgische Encefalomyelitis/ Chronisch Vermoeidheidssyndroom (ME/CVS): een kritische review van onderzoeksmethoden], werd op 1 januari gepubliceerd in Frontiers.
Het artikel van VanElzakker, Brumfield en Mejia is een kritische review van de literatuur over cytokines en neuro-inflammatie in het onderzoek naar ME. Het belangrijkste uitgangspunt van het artikel is dat neurobeeldvorming niet altijd op de juiste manier toegepast wordt om problemen binnen de hersenstam te herkennen, daar waar naar hun mening waarschijnlijk afwijkingen te vinden zijn.
We betogen dat de grote meerderheid van neurobeeldvorming van ME/CVS geen optimale technieken gebruiken om de hersenstam te bestuderen, ondanks de waarschijnlijke centrale rol ervan voor eventuele neuro-inflammatoire oorzaken of autonome effecten.
Ze argumenteren ook dat het omwille van verschillende factoren onwaarschijnlijk is dat er ooit een echt “cytokineprofiel” ontdekt zal worden bij mensen met ME – of in een andere groep personen.
Wat is het probleem met neurobeeldvorming bij ME?
VanElzakker et al. hebben drie potentiële problemen besproken die aangepakt moeten worden om vooruitgang te boeken in het onderzoek naar ME m.b.v. neurobeeldvorming.
- Hoe kan een gemeten component van neuro-inflammatie leiden tot [de] symptomen [die gezien worden bij mensen met ME]?
- Hoe kunnen we die component van neuro-inflammatie accuraat meten?
- Wat kan en kan niet geconcludeerd worden uit de gekozen methode?
Vandaag zullen we het enkel hebben over hun waarnemingen op PET, of positronemissietomografie.
PET-scans
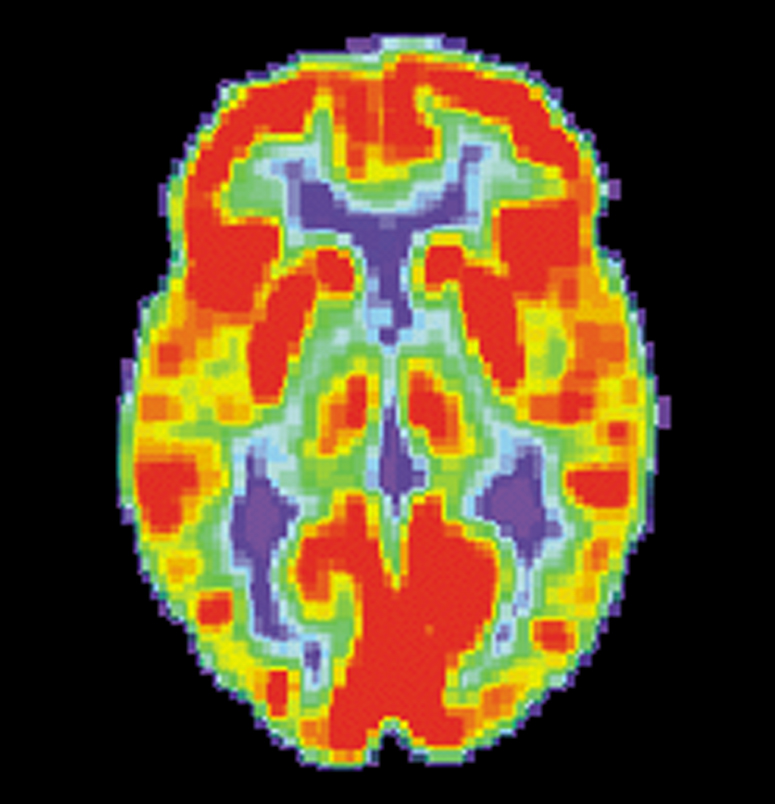
PET-scans zijn een type beeldvorming die gebruikt wordt om metabole processen te onderzoeken, in dit geval die in het centraal zenuwstelsel. Van PET-scans denkt men vaak dat ze meer kans geven om iets te ontdekken dan scans die de arts alleen toelaten om statische morfologie te bekijken. Ze zijn echter ook duurder en daarom is het moeilijker om genoeg financiering te krijgen om de onderzoeker in staat te stellen om statistische significantie te bereiken met hetgeen hij of zij vindt.
De hersenstam is de sleutel
De auteurs argumenteren vervolgens dat traditionele neurobeeldvorming niet bedoeld was om de hersenstam te bestuderen, daar waar de problemen kunnen liggen bij mensen met ME.
Bij het uitvoeren van neurobeeldvorming, vergelijkt software de anatomie van elke deelnemer zijn hersenen met die van anderen. Helaas is de meeste neurobeeldvorming gefocust op de delen van de hersenen die verantwoordelijk zijn voor ‘hogere’ cognitieve processen, en niet voor autonome functie (controle van ademhaling en hartslag bv.), arousal, pijn en neuro-immuunfuncties, die allemaal geassocieerd zijn met de hersenstam. Deze zijn misschien wel enkele van de meest belangrijke dingen om te bestuderen bij mensen met ME.
De hersenstam bestaat uit veel kleine gebieden die verantwoordelijk zijn voor heel verschillende dingen, en kleine beeldvormingsfouten kunnen leiden tot belangrijke interpretatiefouten. De auteurs merken op dat de problemen hoe dan ook opmerkelijk moeten zijn om zichtbaar te zijn, zoals dat het geval was in de beeldvormingsstudie van Nakatomi uit 2014. Software die ervoor zorgt dat hersenstam vergeleken wordt met hersenstam van persoon tot persoon zou ons allicht heel wat vertellen.
De hersenstam pulseert ook bij elke hartslag en is daardoor erg gevoelig voor bewegingsgerelateerde beeldvormingsfouten. Door de hartslag te meten in combinatie met de scan is het mogelijk om dit probleem te compenseren, zoals Barnden et al. deden in hun studie uit 2016. De auteurs merken op dat Barndens studie en ook die van Costa, die specifiek focusten op de hersenstam en geschiktere beeldvormingstechnieken gebruikten, afwijkingen vonden zoals hypoperfusie in de hersenstam.
Gebruik de juiste marker voor neuro-inflammatie
“Radioliganden” zijn radioactieve substanties die zich binden aan bepaalde weefsels en receptoren, waardoor ze worden opgelicht op scans zoals PET. Sommige radioliganden zijn een enkele, radioactieve isotoop – zoals het jodium dat gebruikt wordt om je schildklier in beeld te brengen – en andere zijn eiwitten die aangepast zijn om te binden aan zeer specifieke receptoren.
Nakatomi et al. (2014) gebruikten een radioligand die specifiek afgestemd is op neuro-inflammatie, maar VanElzakker et al. wijzen erop dat de gebruikte ligand niet erg specifiek was – dat wil zeggen dat het gebonden kan zijn aan andere dingen in het lichaam. Ook kan het wat moeite kosten om in de hersenen te geraken, wat de beeldvorming moeilijker maakt.
Er bestaan nu modernere liganden die specifieker zijn en een hogere penetratie hebben.
Hersenen zijn misschien niet perfect gezond op een plaats en merkbaar ontstoken op een andere plaats
De auteurs merken op dat, om neuro-inflammatie te bepalen, de meeste studies één deel van de patiënten hun hersenen vergelijken met een ander deel van de hersenen van dezelfde patiënt: het cerebellum wordt meestal gebruikt als de referentie/controle. Er is echter geen reden waarom er geen algemene toename zou kunnen zijn van neuro-inflammatie bij mensen met ME, waarbij sommige delen van de hersenen meer getroffen zijn dan andere delen. Dit vermindert de kans op het waarnemen van het neuro-inflammatoire ‘signaal’.
Het metabolisme van de radioligand
Meerdere studies hebben nu aangetoond dat mensen met ME een algemeen verschillend metabolisme hebben dan gezonde controles – van het verwerken van suikers versus vetten versus eiwitten, tot algehele metabole snelheid. Als deze preliminaire bevindingen correct zijn, dan kan de radioligand trager gemetaboliseerd worden bij mensen met ME, wat na verloop van tijd leidt tot een accumulatie van de radioligand. Dit probleem kan nog gecompliceerder worden door de slechte penetratie van traditionele radioliganden; het zou kunnen dat meer en meer radioliganden trager opgenomen worden door mensen met ME, maar dat ze mogelijk niet aan dezelfde snelheid afgebroken zouden worden. Hierdoor zou het lijken alsof mensen met ME meer neuro-inflammatie hadden dan gezonde controles, terwijl het in feite een teken van een vertraagd metabolisme zou kunnen zijn.
Modernere radioliganden zouden dit probleem niet volledig elimineren, maar ze zouden het probleem kleiner maken doordat ze de hersenen in beide groepen sneller zouden binnenkomen. De kans dat het zich na verloop van tijd opstapelt bij mensen met ME zou nog steeds bestaan, maar het proportionele verschil zou niet dramatisch zijn. Ten slotte zou het gebruik van lijnbemonstering om te bepalen hoeveel radioligand er “achterblijft” in het bloed op bepaalde intervallen, het probleem bijna volledig kunnen elimineren.
Het binden van de radioligand kan beïnvloed worden de genetische code van de patiënt
Er zijn SNP’s die van invloed kunnen zijn op hoe goed een radioligand aan receptoren bindt; de patiënt zou op deze varianten getest moeten worden vóór een scan.
Dat is het voor vandaag, mensen, maar ik hoop om hun waarnemingen over het MRI-proces binnenkort te bespreken. We zijn erg trots op Paulita’s en Sydneys vooruitgang en op al hun harde werk!
© #MEAction. Vertaling Zuiderzon, redactie Abby, ME-gids.
Front. Neurol., 10 January 2019 | https://doi.org/10.3389/fneur.2018.01033
Neuroinflammation and Cytokines in Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): A Critical Review of Research Methods
Michael B. VanElzakker, Sydney A. Brumfield and Paula S. Lara Mejia
Division of Neurotherapeutics, Massachusetts General Hospital, Harvard Medical School, Boston, MA, United States
Myalgic encephalomyelitis/chronic fatigue syndrome (ME/CFS) is the label given to a syndrome that can include long-term flu-like symptoms, profound fatigue, trouble concentrating, and autonomic problems, all of which worsen after exertion. It is unclear how many individuals with this diagnosis are suffering from the same condition or have the same underlying pathophysiology, and the discovery of biomarkers would be clarifying. The name “myalgic encephalomyelitis” essentially means “muscle pain related to central nervous system inflammation” and many efforts to find diagnostic biomarkers have focused on one or more aspects of neuroinflammation, from periphery to brain. As the field uncovers the relationship between the symptoms of this condition and neuroinflammation, attention must be paid to the biological mechanisms of neuroinflammation and issues with its potential measurement. The current review focuses on three methods used to study putative neuroinflammation in ME/CFS: (1) positron emission tomography (PET) neuroimaging using translocator protein (TSPO) binding radioligand (2) magnetic resonance spectroscopy (MRS) neuroimaging and (3) assays of cytokines circulating in blood and cerebrospinal fluid. PET scanning using TSPO-binding radioligand is a promising option for studies of neuroinflammation. However, methodological difficulties that exist both in this particular technique and across the ME/CFS neuroimaging literature must be addressed for any results to be interpretable. We argue that the vast majority of ME/CFS neuroimaging has failed to use optimal techniques for studying brainstem, despite its probable centrality to any neuroinflammatory causes or autonomic effects. MRS is discussed as a less informative but more widely available, less invasive, and less expensive option for imaging neuroinflammation, and existing studies using MRS neuroimaging are reviewed. Studies seeking to find a peripheral circulating cytokine “profile” for ME/CFS are reviewed, with attention paid to the biological and methodological reasons for lack of replication among these studies. We argue that both the biological mechanisms of cytokines and the innumerable sources of potential variance in their measurement make it unlikely that a consistent and replicable diagnostic cytokine profile will ever be discovered.
Citeren?
VanElzakker MB, Brumfield SA and Lara Mejia PS (2019) Neuroinflammation and Cytokines in Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): A Critical Review of Research Methods. Front. Neurol. 9:1033. doi: 10.3389/fneur.2018.01033





