 Charlotte Stephens, ME Association, 2 december 2019
Charlotte Stephens, ME Association, 2 december 2019
Een recente publicatie door onderzoekers van de Griffith University in Australië onderzocht de mogelijke therapeutische mechanismen van een geneesmiddel, Naltrexone genaamd, bij ME/cvs-patiënten.
In dit samenvattend overzicht leggen we uit wat Naltrexone is, hoe het werkt, waar het voor gebruikt wordt en waarom het nuttig kan zijn als behandeling voor ME/cvs, en we bespreken ook de bevindingen van deze laatste studie.
Belangrijkste punten
- Naltrexone is een opioïdereceptorblokker, die traditioneel gebruikt wordt bij behandeling en herstel van alcohol- en opioïdeverslaving.
- In veel lagere dosissen dan het traditionele gebruik (bekend als Naltrexone in lage dosis of LDN), wordt het ‘off-label’ (onofficieel) gebruikt in de behandeling van een verscheidenheid aan chronische ziekten, waaronder multiple sclerose (MS), reumatoïde artritis, de ziekte van Crohn, fibromyalgie, complex regionaal pijnsyndroom (CRPS) en het syndroom van Sjögren.
- Verschillende studies tonen de doeltreffendheid aan als een inflammatoir, pijnmodulerend geneesmiddel dat nuttig is bij veel auto-immuunachtige aandoeningen.
- De Australische studie wijst erop dat Naltrexone in staat is om de functie in naturalkillercellen (een type immuuncellen waarvan veel studies gevonden hebben dat deze niet goed functioneren bij ME/cvs) te herstellen bij ME/cvs-patiënten. Grotere studies zijn nodig om deze resultaten te valideren.
- In November werd er een retrospectieve studie uit Finland gepubliceerd die gewag maakt van een positieve behandelingsrespons en een goed veiligheidsprofiel voor LDN. Dit was echter geen klinische studie, dus moeten we voorzichtig blijven met de resultaten.
- Dr. Jarred Youngers team in Amerika voert momenteel een klinische studie uit naar het gebruik van LDN bij ME/cvs die normaal in de zomer van 2020 voltooid moet zijn.
Berichten in de media
- Griffith University – Onderzoekers ontdekken mogelijke therapeutische aanpak om ME/cvs te behandelen – 11 november 2019
Wat is Naltrexone?
Naltrexone is een medicijn dat zich bindt aan de opioïdereceptoren van cellen in heel het lichaam en ze blokkeert. Het wordt in eerste instantie gebruikt voor de behandeling van alcohol- of opiatenverslaving, omdat het de effecten van middelen die bekend staan als opiaten (bijv. morfine, codeïne, heroïne), blokkeert en de drang om deze stoffen te gebruiken, vermindert.
Naltrexone in lage dosis (LDN)
© Cptinc.org
Er wordt gesproken van Naltrexone in lage dosis (LDN) wanneer Naltrexone in veel lagere doses wordt genomen dan voor het klassieke gebruik wordt voorgeschreven; meestal rond de 2-10% van de hoeveelheid gebruikt voor de opioïdeverslaving (Toljan et al., 2018).
Men vermoedt dat LDN kan werken als immuunmodulator en heilzaam kan zijn voor een reeks van ontstekingsaandoeningen, waaronder de ziekte van Crohn, multipele sclerose (MS) en fibromyalgie (Patten et al. 2018).
LDN wordt sinds 1985 ‘off-label’ (onofficieel) gebruikt bij de behandeling van een reeks chronische ziekten in de VS, maar is relatief nieuw in het VK en Europa (Ringerike et al. 2015).
Hoewel LDN relatief goedkoop is, is het mogelijk dat er bij de NHS geen subsidie beschikbaar is voor het off-label voorschrijven.
Hoe werkt LDN?
LDN werkt anders dan Naltrexone. Bij lage doseringen blokkeert het maar een paar uur lang de opiaatreceptoren. Als deze geblokkeerd zijn, gaat je lichaam als reactie veel endorfines produceren, onze ‘goed gevoel’-stofjes en onze eigen natuurlijke pijnstillers (opioïden) (Sprouse-Blum et al. 2010).
Een kleine dosis Naltrexone kan de productie van endorfines tot 300% verhogen (Bihari 2013). De hogere waarden van endorfines kunnen tot 12 à 24 uur na inname van het medicijn blijven duren.
Interessant is dat een onderzoek van Conti et al. significant verlaagde niveaus van endorfines bij ME/cvs patiënten rapporteerde, wat een toestand van chronische immuunactivatie aangeeft.
Behalve verhoogde endorfinegehaltes werden nog diverse andere werkingsmechanismen van LDN gerapporteerd, waaronder immuunmodulerende en anti-inflammatoire effecten.
Naltrexone blokkeert de activering van microglia – immuuncellen in het centrale zenuwstelsel die de oorzaak zijn van het vrijkomen van ontstekingsbevorderende cytokines en neuro-inflammatie (Younger et al. 2014).
Deze cellen zijn betrokken bij de pathologie van ME/cvs en zijn ook verantwoordelijk voor ‘ziektegedrag’ (d.w.z. vermoeidheid, griepachtige symptomen, pijn, enz.).
De toegenomen endorfineniveaus moduleren ook de immuunrespons. Ze regelen de productie van T- en B-cellen en herstellen het evenwicht van de T-helper- en T-regulerende cellen, immuuncellen die er voor zorgen dat het immuunsysteem zichzelf niet langer aanvalt (Bihari 2013).
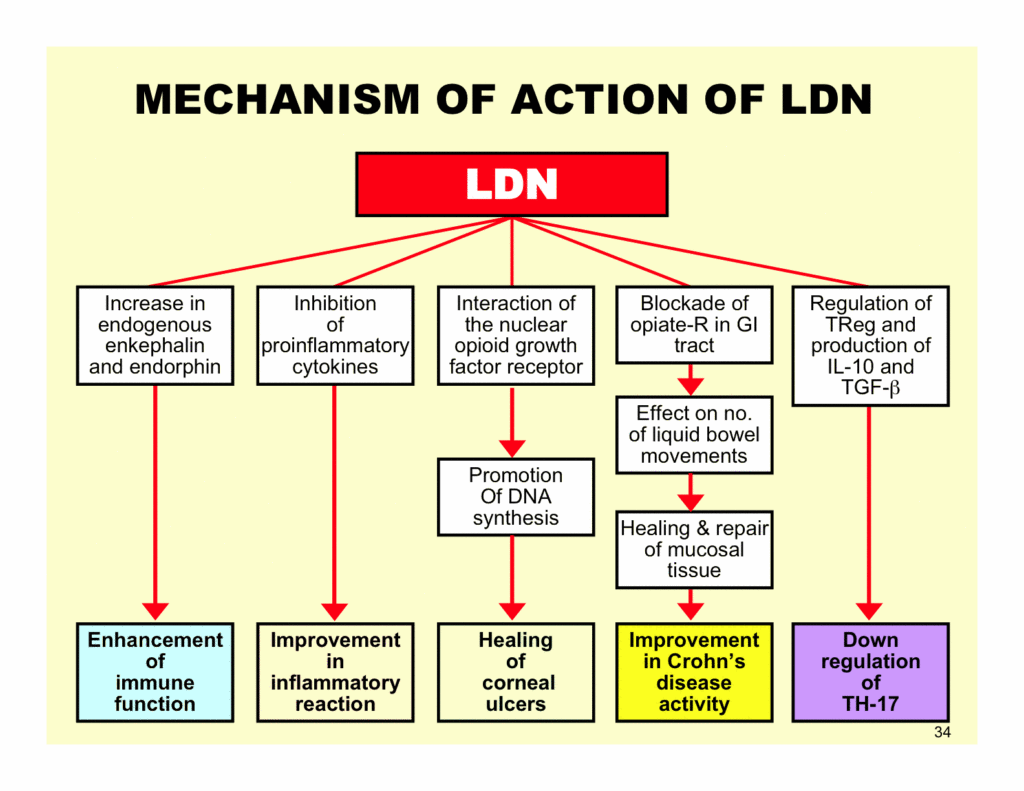
Overgenomen van: Aristo Vojdani, Ph.D.: Mechanismen geassocieerd met LDN-therapie
Bewijzen die het gebruik van LDN bij chronische ziekten onderbouwen
Klinische rapporten over LDN hebben mogelijke baten aangetoond bij veel chronische ziekten zoals fibromyalgie, het syndroom van Sjögren, de ziekte van Crohn, multiple sclerose (MS) en het complex-regionaal pijnsyndroom (CRPS) (Patten et al. 2018).
LDN is een relatief ‘nieuw’ geneesmiddel wat onderzoek betreft: de eerste LDN-studie bij mensen is gepubliceerd in 2007. Sindsdien is LDN in een klein aantal laboratoria onderzocht en heeft het langzaamaan belangstelling gekregen als mogelijke behandeling voor chronische aandoeningen (Younger et al. 2014).
Casestudies, rapporten en onderzoeken tonen aan dat LDN veilig is en goed verdragen wordt. Er zijn echter zeer weinig grote, langlopende gerandomiseerde controlestudies uitgevoerd.
- Zie de referentielijst hieronder voor andere studies met LDN bij diverse ziekten.
Twee kleine verkennende pilootstudies hebben aangetoond dat een behandeling met LDN een doeltreffende, veilige en goedkope behandeling tegen fibromyalgie kan zijn (Metyas et al. 2018).
In een studie bij 47 patiënten met inflammatoire darmziekte, gaf LDN een klinische verbetering bij 75%, en een remissie bij 26% van de patiënten (Lie et al. 2018).
Er is aangetoond dat LDN de behoefte aan medicatie bij patiënten met reumatoïde artritis vermindert (Raknes 2019) en er is zelfs vastgesteld dat het de kwaliteit van leven bij patiënten met de ziekte van Parkinson verbetert (Guttuso et al. 2010).
Verschillende studies hebben aangetoond dat LDN een veilig, goed te verdragen en heilzaam geneesmiddel is voor MS-patiënten (Gironi et al. 2008; Cree et al. 2010; Sharafaddinzadeh et al. 2010).
Resultaten van de retrospectieve studie uit Finland
Een recente studie uit Finland onderzocht de medische gegevens van 218 mensen met ME/cvs die tussen 2010 en 2014 behandeld waren met LDN. Ze keken naar de zelfgerapporteerde feedback van patiënten over eventuele verbeteringen of bijwerkingen en hebben de gegevens gepresenteerd.
Ze vonden dat er een positieve behandelingsrespons gerapporteerd werd bij 74% van de patiënten. Milde bijwerkingen (slapeloosheid, misselijkheid) kwamen vaak voor aan het begin van de behandeling. Geen ernstige bijwerkingen werden gerapporteerd en slechts 7% van de patiënten stopte met LDN vanwege bijwerkingen (meestal misselijkheid).
Er moet echter opgemerkt worden dat dit geen klinische controlestudie was en dus kunnen we hier geen solide conclusies uit trekken of aanbevelingen doen, noch bepalen hoeveel van de respons te wijten was aan het placebo-effect.
De hoge behandelingsrespons, samen met het goede veiligheidsprofiel dat werd waargenomen in deze studie, zou aanleiding kunnen geven tot de ontwikkeling van klinische controlestudies om de haalbaarheid van LDN als een therapeutische geneesmiddel voor ME/cvs te bevestigen.
Het werk van Dr. Jarred Younger
Dr. Jarred Younger heeft in Amerika veel onderzoek gedaan naar LDN en heeft succesvolle klinische proeven verricht bij fibromyalgie (Younger et al. 2014).

Dr Jarred Younger. © uab.edu
In een pilootstudie in 2013 met placebo- en kruiscontrole bij 31 vrouwen met fibromyalgie, verminderde LDN de dagelijkse pijnniveaus, verbeterde het de stemming en de levenskwaliteit (Younger et al. 2013).
Een studie van 2017 vond significante dalingen in niveaus van inflammatoire cytokines na behandeling met LDN gedurende 10 weken bij 8 vrouwen met fibromyalgie (Parkitny and Younger, 2017).
In 2019 vond hij bewijs van neuro-inflammatie bij ME/cvs, en in combinatie met zijn theorie van activering van de microgliale cellen, is zijn team nu ook onderzoek aan het doen naar de therapeutische voordelen van LDN.
Ze zijn momenteel bezig met een klinische studie van LDN bij 30 ME/cvs-patiënten, die in de zomer van 2020 afgerond moet zijn, dus die resultaten zullen zeer interessant zijn!
De Australische studie van LDN voor ME/cvs
“Naltrexone Restores Impaired Transient Receptor Potential Melastatin 3 Ion Channel Function in Natural Killer Cells From Myalgic Encephalomyelitis/Chronic Fatigue Syndrome Patients” [Naltrexone herstelt verstoorde TRPM3-ionkanaalfunctie in naturalkillercellen bij Myalgische Encefalomyelitis/chronisch vermoeidheidssyndroom]
De Australische onderzoekers hebben vroeger al een hypothese naar voren gebracht, die zij gevalideerd hebben met behulp van hun nieuwe patch-clamptechniek om cellen te onderzoeken, en die zegt dat de TRPM3-ionkanaalfunctie van de naturalkillercellen (een type immuuncel) bij ME/cvs verstoord is.
Een slechte werking van dit ionkanaal heeft invloed op de calciumsignalering, die nodig is voor het doeltreffend functioneren van naturalkillercellen (NK).
Verscheidene andere studies hebben ook afwijkingen in naturalkillercellen bij ME/cvs gerapporteerd.
- In 2018 hebben we een beknopt overzicht gemaakt van het onderzoek naar naturalkillercellen bij ME/cvs
In deze recentste studie bestudeerden de onderzoekers de effecten van Naltrexone op de activiteit van het TRPM3-ionenkanaal in NK-cellen afkomstig van ME/cvs-patiënten.
Ze isoleerden NK-cellen van 8 ME/cvs-patiënten en van 8 controles en gebruikten hun ‘gouden standaard patch-clamptechniek van gehele cellen’ (waarbij elektrische stromen door een cel worden geleid en de verandering in stroom wordt gemeten) om de TRPM3-activiteit te meten, na activering met pregnenolonsulfaat.
Vervolgens maten ze de TRPM3-activiteit in NK-cellen die gedurende 24 uur met Naltrexone waren behandeld en ze vergeleken dit met de cellen die niet waren behandeld, om de veranderingen in de ionkanaalactiviteit te bekijken en om te zien wat het effect van Naltrexone was op de ionkanaalfunctie.
Resultaten
In overeenstemming met hun eerdere studies, bevestigden de onderzoekers een “significant verlies van de TRPM3-kanaalactiviteit bij ME/cvs-patiënten” na stimulatie van de NK-cellen, vergeleken met gezonde controles.
Dit onderzoek levert verder bewijs richting TRPM3-kanalen als voorspellende marker en/of een potentieel therapeutisch doelwit voor ME/cvs.
Wat nog meer van belang is: ze ontdekten dat incubatie met Naltrexone (NTX) gedurende 24 uur de TRPM3-kanaalactiviteit in NK-cellen van ME/cvs-patiënten herstelde tot hetzelfde niveau als bij gezonde controles.
Eenvoudig gezegd: het ionkanaal op de NK-cellen van ME/cvs-patiënten reageerde niet in dezelfde mate op stimulering als dat van gezonde controles, maar na behandeling met Naltrexone was de werking van het ionkanaal hersteld tot een normaal niveau (zie figuur 1). Dit betekent dat ook de functies van de NK-cellen hersteld zouden moeten zijn.
“Onze nieuwe bevindingen geven dus aan dat NTX het potentieel heeft om de TRPM3-kanaalactiviteit bij ME/cvs-patiënten te herstellen, met als resultaat een hermodellering van het Ca2+-signaal, wat op haar beurt weer een invloed heeft op de celfuncties. Dit staaft de hypothese dat NTX mogelijk kan worden gebruikt voor de behandeling van ME/cvs”.
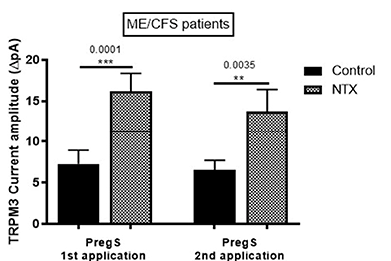
Figuur 4I. Toont het werkingsniveau van het ionenkanaal bij NK-cellen die met Naltrexone (NTX) behandeld zijn (grijze balk) in vergelijking met cellen die er niet mee behandeld zijn (zwarte balk), na opeenvolgende stimulering met Preg S. Er is een significant verschil tussen de twee: de cellen die met Naltrexone behandeld zijn, vertonen een veel grotere reactie op de stimulering en laten zien dat Naltrexone de activiteit van de ionenkanalen hersteld heeft. © Cabanas et al., 2019.
Aandachtspunten
-
Het was een kleine studie: slechts 8 ME/cvs-patiënten waren erin opgenomen. Dit betekent dat het moeilijk is om conclusies te trekken en dat het onderzoek moet worden herhaald met een veel groter cohort.
-
Laboratoriumomstandigheden: de studie keek naar cellen die geïsoleerd werden bekeken, nadat er veel bewerkingen en elektrische stromen door de cellen waren gejaagd en verschillende chemicaliën waren toegediend om ze te activeren of af te remmen. Dit betekent dat het geen afspiegeling is van de omstandigheden in het lichaam en dat het dus moeilijk te zeggen is of deze resultaten, waargenomen in laboratoriumomstandigheden, in het lichaam gerepliceerd zouden worden.
-
Dosering van Naltrexone: cellen werden 24 uur lang met Naltrexone geïncubeerd, wat niet zou gebeuren bij inname van de medicatie in het ‘echte leven’, en het is niet duidelijk wat de werkelijke dosering hiervan in het echte leven zou kunnen zijn.
-
Om te bepalen of Naltrexone veilig en heilzaam is voor ME/cvs-patiënten, moeten er klinische studies op grote schaal en op lange termijn uitgevoerd worden.
Commentaar van Dr. Charles Shepherd, Medisch Ere-Adviseur van de ME Association
“Dit is een kleine, maar interessante in een laboratorium uitgevoerde onderzoeksstudie. Het zou echter voorbarig zijn om deze bevindingen te extrapoleren naar de conclusie dat naltrexone waarschijnlijk een veilige en doeltreffende vorm van medicamenteuze behandeling is voor ME/cvs.”
“We hebben zeer gemengde feedback ontvangen van mensen hier in het VK die naltrexone hebben gebruikt – hoewel het geen goedkeuring heeft voor de behandeling van ME. Hoewel sommige mensen voordelen melden, doen anderen dat niet – mogelijk omdat naltrexone voor een aantal nevenwerkingen kan zorgen die overlappen met de symptomen van ME/cvs.”
“We hebben de mogelijkheid onderzocht om financiering te bieden voor een kleine klinische studie van naltrexone met een onderzoeker in het VK, maar er is geen subsidieaanvraag ontvangen.”
“Bij gebrek aan degelijk bewijs van zowel werkzaamheid als veiligheid, is dit daarom met onze huidige staat van kennis geen geneesmiddel dat aanbevolen kan worden voor gebruik bij ME/cvs, buiten in het kader van een wetenschappelijk onderzoek.”
Conclusie
Deze laatste studie toont aan dat Naltrexone kan helpen bij het herstellen van immuundisfunctie op cellulair niveau en ze levert ook bijkomend bewijs van afwijkingen bij naturalkillercellen.
LDN zou een veelbelovende therapeutische optie kunnen worden om de levenskwaliteit van sommige personen te helpen verbeteren. Er zijn echter grote klinische studies nodig om de veiligheid en werkzaamheid van LDN bij ME/cvs te testen.
We zien de resultaten van de klinische studie van Dr. Jarred Younger met belangstelling tegemoet, in de hoop dat ze meer duidelijkheid zullen verschaffen.
Om meer te weten te komen over Naltrexone in lage dosis (LDN):
- LDN Research Trust [in het Engels, n.v.d.r.]
- LDN Science [in het Engels, n.v.d.r.]
- Forumdraad ME-gids over LDN
- ME(cvs) Wetenschap over Naltrexon
Referenties
Bihari B (2013) Bernard Bihari, MD: low-dose naltrexone for normalizing immune system function. Altern Therp Health Med. 19: 56-65.
Chopra P and Cooper M (2013) Treatment of Complex Regional Pain Syndrome (CRPS) Using Low Dose Naltrexone (LDN) Journal of Neuroimmune Pharmacology 8 (3): 470-476.
Conti F, Pittoni V, Sacerdote P, Priori R, Meroni PL, Valesini G. Decreased immunoreactive beta-endorphin in mononuclear leucocytes from patients with chronic fatigue
syndrome. Clin Exp Rheumatol. (1998) 16:729–32.
Cree BA, et al. (2010) Pilot trial of low-dose naltrexone and quality of life in multiple sclerosis. Annals of Neurology 68(2):145-150.
Gironi M, et al. (2008) A pilot trial of low-dose naltrexone in primary progressive multiple sclerosis. Multiple Sclerosis 14(8):1076-1083.
Guttuso T et al. (2010) Abstract #13: Low-Dose Naltrexone’s Tolerability and Effects in Fatigued Patients with Parkinson’s Disease: An Open-Label Study Neurotherapeutics 7 (3): 332.
Hammer L et al. (2016) Opioid growth factor and low-dose naltrexone impair central nervous system infiltration by CD4+ T lymphocytes in established experimental autoimmune encephalomyelitis, a model of multiple sclerosis. Exp Biol Med (Maywood) 241(1):71-78.
Kariv R et al. (2006) Low-dose naltreoxone for the treatment of irritable bowel syndrome: a pilot study. Dig Dis Sci 51 (12): 2128-2133.
Ludwig M et al. (2017) P. Serum [Met5]-enkephalin levels are reduced in multiple sclerosis and restored by low-dose naltrexone. Exp Biol Med (Maywood) 242(15):1524-1533.
Ludwig MD, et al. (2016) Long-term treatment with low dose naltrexone maintains stable health in patients with multiple sclerosis. Multiple Sclerosis Journal – Experimental, Translational and Clinical 2:1-11.
Lie MRKL et al. (2018) Low dose Naltrexone for induction of remission in inflammatory bowel disease patients. Journal of Translational Medicine 16 (1): 55.
Metyas S et al. (2018) Low Dose Naltrexone in the Treatment of Fibromyalgia. Current Rheumatology Reviews 14 (2): 177-180.
Parkitny L, Younger J. (2017) Reduced pro-inflammatory cytokines after eight weeks of low- dose naltrexone for fibromyalgia. Biomedicines 5(2).
Patten DK et al. (2018) The Safety and Efficacy of Low-Dose Naltrexone in the Management of Chronic Pain and Inflammation in Multiple Sclerosis, Fibromyalgia, Crohn’s Disease, and Other Chronic Pain Disorders. Pharmacotherapy 38 (3): 382-389.
Raknes G (2019) Low dose naltrexone: Effects on medication in rheumatoid and seropositive arthritis. A nationwide register-based controlled quasi-experimental before-after study. PLoS One 14 (2).
Ramanathan S et al. (2012) Is fibromyalgia an endocrine/endorphin deficit disorder? Is low dose naltrexone a new treatment option? Psychosomatics 53 (6): 591-4.
Ringerike T, Pike E, Nevjar J, Klemp M. (2015) The Use of Naltrexone in Low Doses Beyond the Approved Indication. Oslo: Report from Norwegian Knowledge Centre for the Health Services (NOKC)
Schwaiger T (2018) The Uses of Low-Dose Naltrexone in Clinical Practice: Potential benefits for a wide range of conditions. Natural Medicine Journal 10 (4)
Segal D et al. (2014) Low dose naltrexone for induction of remission in Crohn’s disease. Cochrane Database Syst Rev. (2):CD010410.
Sharafaddinzadeh N, et al. (2010) The effect of low-dose naltrexone on quality of life of patients with multiple sclerosis: a randomized placebo-controlled trial. Multiple Sclerosis 16(8):964-969.
Smith JP et al. (2013) Safety and tolerability of low-dose naltrexone therapy in children with moderate to severe Crohn’s disease: a pilot study. J Clin Gastroenterol 47(4):339-345.
Smith JP et al. (2017) Low-dose naltrexone therapy improves active Crohn’s disease. Am J Gastroenterol 102(4):820-828.
Sprouse-Blum AS et al. (2010) Understanding endorphins and their importance in pain management. Hawaii Med J. 69(3):70-71.
Toljan K et al. (2018) Low-Dose Naltrexone (LDN)-Review of Therapeutic Utilization. Medical Science 6 (4).
Weinstock LB et al. (2016) Identification and Treatment of New Inflammatory Triggers for Complex Regional Pain Syndrome: Small Intestinal Bacterial Overgrowth and Obstructive Sleep Apnea. A A Case Reports 6 (9): 272-276.
Younger J and Mackey S. (2009) Fibromyalgia symptoms are reduced by low-dose naltrexone: a pilot study. Pain Med. 10(4):663-672.
Younger J et al. (2013) Low-dose naltrexone for the treatment of fibromyalgia: findings of a small, randomized, double-blind, placebo-controlled, counterbalanced, crossover trial assessing daily pain levels. Arthritis Rheum. 65(2):529-538.
Younger J et al. (2014) The use of low-dose naltrexone (LDN) as a novel anti-inflammatory treatment for chronic pain. Clin Rheumatol. 33(4):451-459.
Zashin S (2019) Sjogren’s Syndrome: Clinical Benefits of Low-dose Naltrexone Therapy. Curesus 11 (3).
© ME Association. Vertaling Els en Zuiderzon, redactie Abby en Zuiderzon, ME-gids.
Opnieuw gepubliceerd met vriendelijke toestemming van de Britse ME Association.
Engelse versie beschikbaar op hun website: www.measociation.org.uk





