Cort Johnson, Simmaron Research, 10 mei 2020
Sleutelwoorden, tags: B2Adr, bloedvolume, sympathisch zenuwstelsel
Dit is een andere hypothesepaper die hoop geeft – en waarbij je je afvraagt of de auteurs misschien wel grip hebben op wat er gebeurt met het ME/cvs. Het artikel stelt dat een prikkelend eenvoudig probleem – een auto-immuunaanval op slechts één receptor – uit honderden potentiële receptoren – vrijwel alle symptomen van ME/cvs zou kunnen veroorzaken: B2AdR
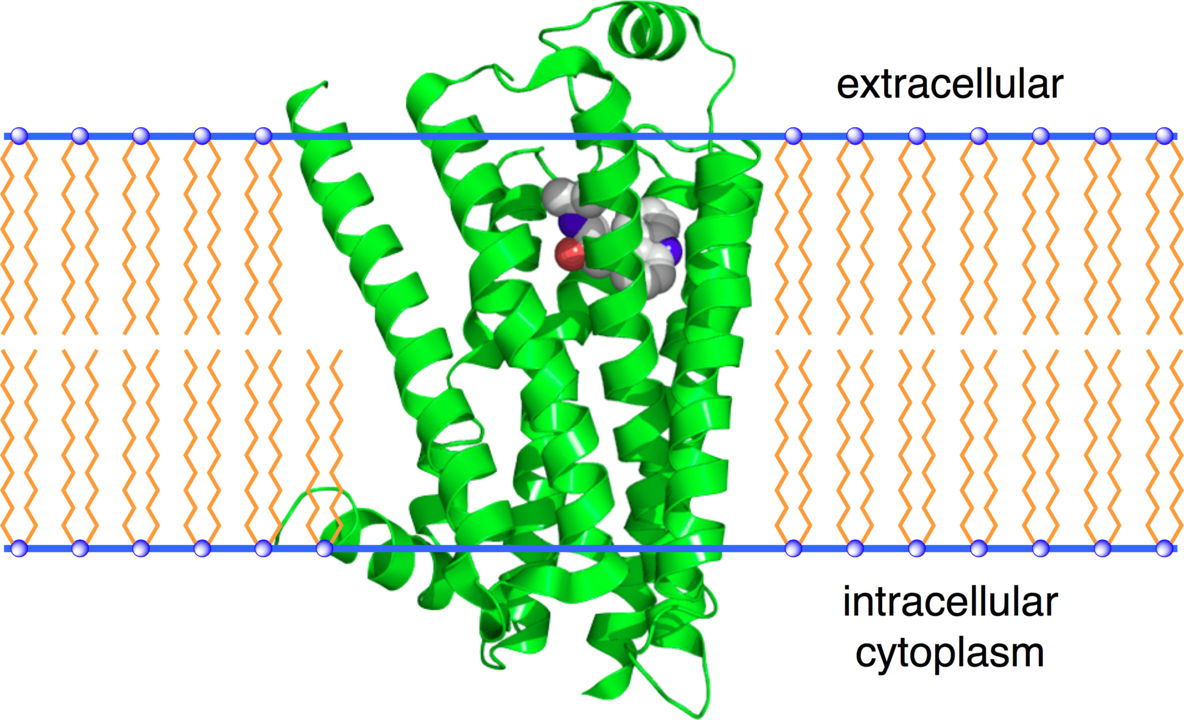
Kan een auto-immuunproces dat de B2-adrenerge receptor aanvalt, de symptomen van ME/cvs veroorzaken?
Receptoren die het oppervlak van een cel aanstippen, lijken niet indrukwekkend, maar ze zijn eigenlijk de sleutel tot de activiteit van onze cellen. Vergrendel je op een receptor en je laat de cel veranderen. De meeste geneesmiddelen richten zich niet op cellen – ze richten zich op de receptoren op cellen.
Zou slechts één verknipte receptor de symptomen van ME/cvs kunnen veroorzaken? Als het een voldoende belangrijke receptor is die op voldoende plaatsen wordt gevonden – ja, dan kan het, en de receptor in kwestie in dit artikel – is de bèta-2-adrenerge receptor (B2AdR). B2AdR is inderdaad een zware receptor.
B2AdR wordt gevonden in de bloedvaten in de hersenen, de skeletspieren en het hart. Het is een stroomafwaartse bemiddelaar van het sympathische zenuwstelsel (vecht- of vluchtsysteem) dat onder andere de bloedstromen regelt.
Het bewijs voor B2AdR-disfunctie bij ME/cvs neemt toe. Het is niet overweldigend – het is geen uitgemaakte zaak, maar het wijst in een zeer intrigerende richting.
Een studie van een medewerker van het Simmaron-onderzoeksteam, heeft verhoogde niveaus van B2AdR-autoantilichamen (antilichamen die de receptor aanvallen) bij ME/cvs gevonden. Een volgende studie is mogelijk onderweg. Er zijn ook kleine mutaties gevonden in de genen die de receptoren produceren. Bovendien zijn vergelijkbare mutaties ook geassocieerd met een soort milde ME/cvs-achtige toestand. Ten slotte suggereert het werk van Scheibenbogen dat ß2AdR-autoantilichamen de ß2R-signalering stimuleren, maar bij een subgroep van ME/cvs-patiënten is hun functioneren afgestompt.
Simmaron Research werkte samen met Carmen Scheibenbogen in een pilootonderzoek naar B2AdR-autoantilichamen bij ME/cvs door patiëntenmonsters en financiering bij te dragen in 2018.
Verenigende hypothese?
Dat was genoeg bewijs voor dokter Klaus Wirth en dokter Carmen Scheibenbogen in Duitsland om te geloven dat ze het woord moesten verspreiden en daarmee een grootse, inderdaad een “verenigende” hypothese van ME/cvs opbouwden en publiceerden.
A Unifying Hypothesis of the Pathophysiology of Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): Recognitions from the finding of autoantibodies against ß2-adrenergic receptors. Klaus Wirtha, Carmen Scheibenbogen, Autoimmunity Reviews, 2020
Talloze gedocumenteerde problemen bij ME/cvs, waaronder lage hartslagvariabiliteit, chronotrope incompetentie (onvermogen van de hartslag om op de juiste manier te verhogen tijdens inspanning), iets dat QTc-verkorting wordt genoemd (verkorte ventriculaire repolarisatie) komen hier samen.
De ß2AdR’s in de bloedvaten spelen een belangrijke rol bij het openen of verwijden van de bloedvaten tijdens het sporten om tot 20-voudige toename van de bloedstromen op te vangen die de spieren bereiken. Om dit te doen, geven de bloedvaten een grote verscheidenheid aan vaatverwijdende middelen af, zoals adenosine, ATP, prostaglandines, (PGE’s), prostacycline (PCI), bradykinine (BK) en protonen.

Carmen Scheibenbogen bestudeert al jaren autoantilichamen bij ME/cvs
Tijdens inspanning moet het lichaam ook bloed naar de actieve gebieden sturen en het wegleiden van gebieden die in rust zijn. De slagaders klemmen naar beneden om het bloed krachtig naar de kleine bloedvaten in de spieren te sturen, die op hun beurt moeten openen om de grote hoeveelheden bloed die ze nodig hebben te ontvangen en te gebruiken. Dit proces waarbij de bloedvaten aan het ene uiteinde worden vastgeklemd en aan het andere uiteinde worden geopend, wordt ‘functionele sympatholyse’ genoemd.
De auteurs zijn van mening dat de verhoogde activiteit van het sympathische zenuwstelsel de slagaders stevig vasthoudt. Ondertussen schaadt de B2AdR-disfunctie het vermogen van de kleine bloedvaten om te verwijden. Dit onevenwicht tussen vaatvernauwende en vaatverwijdende krachten – waarbij de vaatvernauwers winnen – veroorzaakt de afgifte van pijnlijke vaatverwijdende stoffen in een poging de bloedvaten te openen. Het hele proces wordt op zijn beurt versterkt door de metabole/energetische problemen in de spieren.
In wat lijkt op een ruw bloedvatequivalent (d.w.z. het lekkende kleine bloedvatsyndroom?) Lekt deze enorme productie van vaatverwijdende middelen in de interstitiële ruimtes tussen de bloedvaten, de lymfe en de cellen. Dit gebeurt omdat een van deze middelen, bradykinine, ook behoorlijk goed is in het verbeteren van de permeabiliteit van microvasculaire (kleine) bloedvaten. Dus nu heb je een aantal krachtige peptiden op een plek die ze niet zouden moeten zijn – wat altijd een recept is voor problemen.
Gooi dat samen met een gebrekkig energieproductiesysteem in de spieren en je hebt een driedubbel probleem. De spieren produceren onvoldoende energie, in wat een zuurstofarme (hypoxische) omgeving lijkt te zijn. De grotere bloedvaten daarentegen worden stevig vastgeklemd. De kleine bloedvaatjes die in het midden vastzitten, pompen een heleboel vaatverwijders uit die, wanneer ze in de weefsels lekken, een prijs vragen.
Dit proces vindt plaats bij dysmenorroe (menstruatiekrampen) wanneer weefsels in een hypoxische (zuurstofarme) en hypersamentrekkende baarmoeder vaatverwijders in het bloed gieten, wat vermoeidheid, griepachtige symptomen, koorts, pijn en zelfs slaapstoornissen veroorzaakt. (Dysmenorroe of endometriose is verhoogd gevonden bij ME/cvs.)
De situatie is een beetje anders bij ME/cvs – de auteurs geloven dat het de bloedvaten zijn die hypercontractiel zijn – niet de spieren. Nu de vaatverwijdende middelen uitstromen, geloven de auteurs zelfs niet dat de spieren bij ME/cvs zich noodzakelijkerwijs in een sterk hypoxische toestand bevinden.
Als een hypercontractiele of hypoxische baarmoeder echter slecht klinkt, overweeg dan hoe hypoxische, hypercontractiele bloedvaten in de skeletspieren door het hele lichaam kunnen zijn – misschien zoiets als ME/cvs.
Afwijkende cardiovasculaire bevindingen
De auteurs stellen voor dat ß2AdR-disfunctie ook verantwoordelijk zou kunnen zijn voor de afwijkende cardiovasculaire situatie die wordt aangetroffen bij ME/cvs. De auteurs noemden de cardiovasculaire bevindingen bij ME/cvs “uniek en niet gevonden in een andere aandoening of ziekte”: hypovolemie (laag bloedvolume), verminderde vullingsdruk (verminderde bloedtoevoer naar het hart), lage cardiale output in rust, kleine harten en als klap op de vuurpijl een lage activiteit van het renine-angiotensine-aldosteronsysteem (RAAS).
Een grote en nooit beantwoorde – en zelden gestelde – vraag over ME/cvs is: waarom is het bloedvolume laag? Dat roept een andere, meer recent gestelde maar vergelijkbare vraag op: waarom worden laag veneuze bloedstromen naar het hart ook consistent gevonden? Met andere woorden, waar is het ontbrekende bloed gebleven?
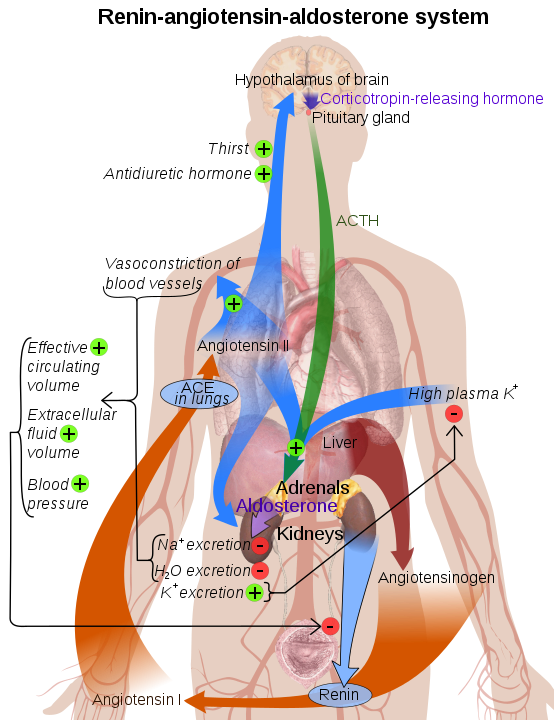
Een traag RAAS-systeem bij ME/cvs is een mysterie gezien het lage aanwezige bloedvolume. De auteurs denken te weten waarom.
Het is een belangrijke vraag. Om te beginnen kan een laag bloedvolume alleen al het sympathische zenuwstelsel in overdrive brengen en de nervus vagus (het rust- en verteringssysteem) in slaap wiegen.
Het echte mysterie is echter wat er aan de hand is met het renine-angiotensine-aldosteronsysteem (RAAS) bij ME/cvs. Lage bloedvolumes zouden dat systeem automatisch moeten activeren om de bloedvolumes te verhogen, maar paradoxaal genoeg lijkt de RAAS-activiteit in plaats van te worden verhoogd, te verminderen bij deze ziekte.
Omdat, zoals hierboven opgemerkt, een laag bloedvolume het sympathische zenuwstelsel in overdrive brengt, kan het onvermogen van de RAAS om zijn werk te doen, een belangrijke rol spelen bij ME/cvs. Om de een of andere reden is bij deze ziekte nauwelijks naar RAAS gekeken.
Wirth en Scheibenbogen hebben zeker gekeken. Ze wendden zich opnieuw tot een vaatverwijder – bradykinine – voor een mogelijk antwoord. Terwijl bradykinine probeert de bloedvaten te openen, kan het tegelijkertijd de RAAS-activiteit en de verhoging van het bloedvolume remmen.
Het overloopeffect
De auteurs geloven niet dat deze problemen alleen in de spieren voorkomen. Ze geloven dat zowat elk symptoom bij ME/cvs kan worden veroorzaakt wanneer vaatverwijdende stoffen in de algemene bloedsomloop terechtkomen, rond de spieren, de lymfeklieren, de darmen en de blaas.
Mits voldoende van deze vaatverwijdende stoffen aanwezig zijn, kan elke belasting van het cardiovasculaire systeem leiden tot vermoeidheid, pijn, griepachtige systemen enz.
Zelfs mentale stress zou volgens hen pijn kunnen veroorzaken doordat het sympathische zenuwstelsel de bloedvaten van de skeletspieren verder naar beneden drukt, waardoor ze vaatverwijders uitzenden in een poging meer bloed te krijgen en pijn, griepachtige symptomen veroorzaken. enz. Voor mij persoonlijk kan dit de spierpijn en griepachtige symptomen verklaren die ik vaak ervaar als ik gewoon in een stoel zit terwijl ik mentaal werk doe.
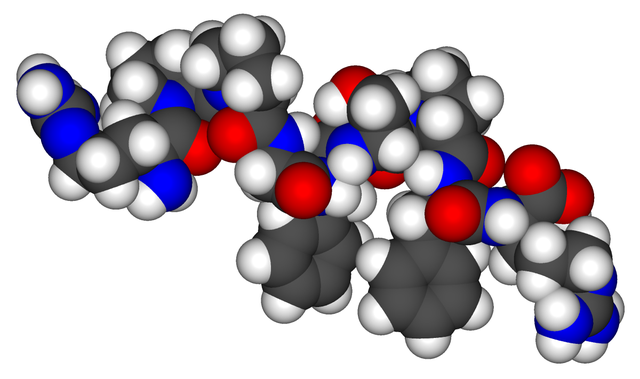
De auteurs concentreerden zich op bradykinine – een vaatverwijder die ook pijn kan veroorzaken en de vasculaire permeabiliteit kan vergroten.
De belangrijkste vaatverwijder – bradykinine – een schijnbaar universele peptide, kan ook de bloed-hersenbarrière openen en bijdragen aan de intracraniële hypertensie, dunnevezelneuropathie, slaapapneu en slaapproblemen. Gezien het lage bloedvolume en de verstoorde vullingsdruk, voorspeld door de overloop van vaatverwijdende stoffen, zou orthostatische intolerantie (problemen met staan) een natuurlijke uitkomst zijn.
Een bijkomende factor bij ME/cvs kan een disfunctie zijn van de endotheelcellen langs de bloedvaten. Autoantilichamen tegen B2AdR-receptoren kunnen ervoor zorgen dat de bloedvaten bij ME/cvs onvoldoende verwijden.
De chroniciteit van dit alles zou ook een rol kunnen spelen. Bij voldoende cardiovasculaire belasting verdwijnen de B2AdR-receptoren gewoon.

Een reportage van de lokale tv wekte de interesse van Klaus Wirth in ME/cvs
Nobele Onbekende
Maar hoe zit het met Klaus Wirth? We hebben zijn naam nog nooit gehoord, maar hier is hij de coauteur van een belangrijke hypothesepaper over ME/cvs. Wirth is, zo blijkt, een experimenteel farmacoloog gericht op cardiovasculair onderzoek in Sanofi-Aventis Deutschland in Frankfurt.
Tijdens zijn onderzoek naar ziekten van kleine bloedvaten realiseerde hij zich hoe belangrijk activering van de bèta-adrenerge receptoren was voor de bloedstromen door zowel de kleine als de grote bloedvaten. In 2018 suggereerde zijn werk dat bèta-adrenerge activering een cruciale rol speelt in de bloedstroom in de hersenen.
In maart 2018 zette hij toevallig een tv-programma aan:
“In maart 2018 zag ik een kort bericht op onze lokale tv zender, over een vader wiens zoon bedlegerig was door ME/cvs. Hij werd geïnterviewd voor zijn activiteiten in de politiek om de financiering voor ME/cvs-onderzoek te vergroten. Ik had geen idee wat ME/cvs was en ik deed die avond een Google-zoekopdracht. De volgende dag ging ik op zoek in pubmed. Het tweede abstract dat ik zag was dat van Carmens groep over autoantilichamen tegen ß2-adrenerge receptoren. Ik voelde meteen dat er een probleem zou kunnen zijn met cerebrale en skeletspierperfusie en een fundamenteel en onderliggend cardiovasculair probleem. Hoewel ik meteen voelde dat ik de pathofysiologie zou kunnen begrijpen, was het erg vermoeiend om de stukjes van deze puzzel bij elkaar te leggen. Het kostte ons 1-1,5 jaar.”
Conclusie
Gezien het enorme bereik van het cardiovasculaire systeem is het een natuurlijke plaats om naar een oorzaak van ME/cvs te zoeken, maar niemand heeft er eerder zo naar gekeken bij ME/cvs-patiënten. Voortbouwend op studies die aantonen dat autoantilichamen tegen de B2AdR-receptoren aanwezig zijn in een significante subgroep van ME/cvs-patiënten, tekenen de auteurs een uitgebreid model van cardiovasculaire disfunctie dat veel, zo niet alle, symptomen van ME/cvs zou kunnen veroorzaken.
In de kern is de hypothese eenvoudig: er is een onevenwicht tussen vaatvernauwing en vaatverwijding in de bloedvaten. Het begint met een vaatvernauwing die wordt veroorzaakt door een overactief sympathisch zenuwstelsel. Schade aan BSAdR-receptoren zorgt ervoor dat de kleine bloedvaten in de buurt van de spieren moeite hebben om voldoende open te gaan om het bloed te krijgen dat ze nodig hebben. Met beperkte bloedstromen en met de energiearme spieren die schreeuwen om meer bloed, zien de auteurs pijn en vermoeidheid die vasodilatatoren uitlokken in een poging die bloedvaten te openen.
Zoveel vaatverwijdende middelen stromen uit dat ze in de algemene circulatie terechtkomen en in de interstitiële ruimtes lekken – de ruimtes tussen de bloedvaten, de lymfe en de weefsels – die pijn, vermoeidheid en andere symptomen veroorzaken – evenals een laag bloedvolume, verstoorde vullingsdruk [het onvoldoende vullen van de kamers van het hart, n.v.d.r.] en hyperactiviteit van het sympathische zenuwstelsel.
Eén vaatverwijder, bradykinine, kan verantwoordelijk zijn voor tal van effecten, waaronder het onvermogen van het renine-angiotensine-aldosteronsysteem om het bloedvolume op het juiste niveau te brengen, intracraniële hypertensie, dunnevezelneuropathie, slaapapneu en slaapproblemen.
Het is inderdaad een grootse, verenigende hypothese. De auteurs zien in feite drie mechanismen waarmee deze bèta-adrenerge receptoren bij ME/cvs kunnen worden beschadigd: autoantilichamen (auto-immuunaanval), polymorfismen (bijv. mutaties) in het gen dat de receptor produceert en desensibilisatie voor chronische cardiovasculaire belasting. Bovendien kunnen problemen met het endotheel (gladde spiercellen langs de bloedvaten) of een andere vorm van vasculaire disfunctie ook sterk bijdragen.
Houd dit onderwerp in de gaten. Er is een tweede hypothesepaper op komst die zich richt op de energieproblemen in de spieren.
© Simmaron Research. Vertaling Linda, redactie Zuiderzon en Abby, ME-gids.






Eén reactie
Interessant artikel,heeft ook raakvlakken met cmd: coronaire microvasculaire dysfunktie.De kleinste vaatjes in het hart funtioneren dus niet goed,terwijl zij verantwoordelijk zijn voor 90% van de zuurstofvoorziening in het hart..In Maastricht gaan ze nu de kleinste vaatjes in rest van het lichaam onderzoeken,denk aan ogen,vingers .Beschadigingen van de vaatjes kan komen door hoge bloeddruk maar ook door ontstekingen in het lichaam