De kernpunten
- Wat kwam de presentatie van dr. Da Silva over „Het in kaart brengen van klinische fenotypes en disfunctie van de HPA-as bij ME/cvs” op de IACFS/ME-conferentie van 2025 toch op het juiste moment. We hebben net gehoord van een hele reeks onderzoeken die de vinger rechtstreeks in de richting van de hersenen lieten wijzen, en nu hebben we een autopsierapport over de hersenen bij ME/cvs.
- Het is bijna zeven jaar geleden dat Health Rising voor het laatst verslag deed van autopsierapporten bij ME/cvs. Een belangrijk thema was dorsale wortelganglionitis – schade aan de neuronen die sensorische signalen naar het ruggenmerg doorgeven.
- Eerdere hersenautopsies concentreerden zich meer op de hersenstam, maar deze groep, die gespecialiseerd is in de hypothalamus, begon bij de HPA-as, die haast vanaf aanvang een aandachtspunt is geweest in het ME/cvs-onderzoek. Waarom? Omdat de HPA het belangrijkste systeem is voor reactie op stress en regulering van energie in het lichaam.
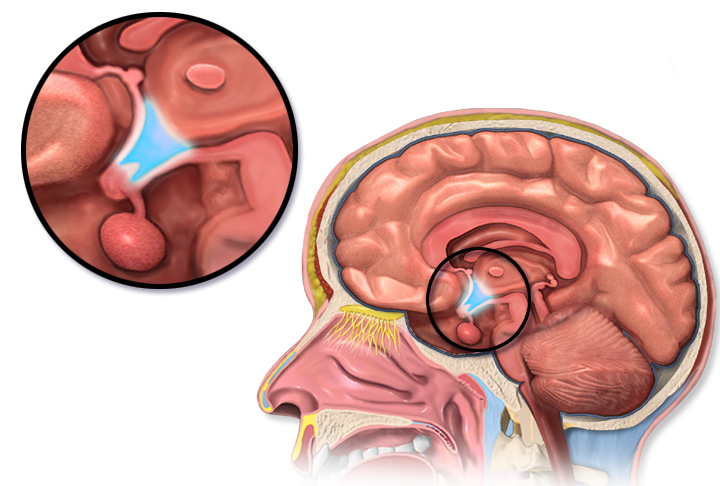
- De hypothalamus, gelegen aan de onderkant van de hersenen, registreert stress, bloedsuikerspiegels, inflammatie, geeft corticotropine-‘releasing’ hormoon (CRH) af aan de hypofyse, die vervolgens cortisol produceert, ook wel de ‘stress- en energiemanager’ van ons lichaam genoemd.
- Cortisol zorgt voor meer energie door de bloedsuikerspiegel te verhogen en helpt ons vet en eiwitten te verbruiken bij het ontwaken en tijdens stressvolle periodes. Het helpt ons ook alert en gefocust te blijven, en in staat te zijn om te reageren op bedreigingen of uitdagingen. Daarnaast is het een belangrijke ontstekingsremmer, helpt het de bloedvaten te vernauwen en heeft het invloed op het geheugen, de aandacht, de motivatie en de stemming.
- De Nederlandse groep telde de neuronen in de hypothalamus, voerde een genexpressieanalyse van de hypofyse uit en onderzocht de cortisolspiegels. Gezien de lagere cortisolspiegels verwachtten ze een toename van het aantal neuronen in de hypothalamus om de productie van CRH op te voeren. Het was allemaal vrij eenvoudig, dachten ze.
- Er was echter iets heel anders aan de hand. In plaats van meer CRH-producerende neuronen vonden ze bij de ME/cvs-patiënten bijna geen CRH-producerende neuronen. Dat suggereerde dat er een algemene onderdrukking van de hypothalamus had plaatsgevonden, maar de vasopressine- en oxytocine-neuronen in de hypothalamus werden ofwel in verhoogde ofwel in normale aantallen aangetroffen. Alleen de CRH-producerende neuronen waren aangetast…
- Een genexpressieanalyse leverde meer bewijs op voor problemen met de HPA-as: de receptoren in de hypofyse die bedoeld waren om te reageren op talrijke neuropeptiden, waren neerwaarts gereguleerd.
- Alles bij elkaar leek de HPA-as, met de drastische afname van CRH-producerende neuronen in de hypothalamus, een uitval van de hypofyse en de waargenomen lagere cortisolspiegels, bij deze postmortaal onderzochte patiënten, vrijwel volledig beschadigd.
- Merk op dat dit mogelijk een zeer ernstig eindstadium van ME/cvs vertegenwoordigt. Het ging om slechts zeven autopsies, en houd er rekening mee dat mensen met een minder ernstig ziekteverloop mogelijk meer functionele CRH-neuronen over hebben.
- Da Silva deed geen uitspraken over de oorzaak. In 2020 stelde Angus Mackay echter op nogal onheilspellende wijze – aan de hand van een gedachte-experiment – dat de “stressintegrator” in de hypothalamus, de paraventriculaire kern (PVK) genaamd, wellicht een sleutelrol speelt bij ME/cvs. De PVK blijkt namelijk de belangrijkste producent van CRH te zijn.
- Mackay stelde dat een ontstoken PVK misschien te veel CRH produceert. Hoewel deze studie een laag aantal CRH-producerende neuronen aantoonde, zou Mackays scenario van een hyperactieve PVK kunnen leiden tot langdurige schade en het uiteindelijk verdwijnen van die neuronen.
- De situatie lijkt maar al te vertrouwd: het is weer een andere versie van het ‘wired and tired’ / ‘burn-out maar vastzittend in dreigingsmodus’-probleem dat deze ziekten lijkt te beheersen.
- De recente (nog niet gepubliceerde) bevinding over noradrenaline (NA) die in een recente blog aan bod kwam, zou hiermee verband kunnen houden. Dichte strengen van noradrenerge (noradrenaline-producerende) vezels vanuit de locus caeruleus reiken rechtstreeks tot in de PVK, waar ze de CRH-productie activeren. Hyperactieve NA-neuronen zouden CRH-neuronen in de hypothalamus kunnen activeren, waardoor deze bij de meest ernstige patiënten uiteindelijk uitgeput raken.
- Deze bevindingen verklaren waarom het toedienen van cortisol in de vorm van een lage dosis hydrocortisone soms negatieve effecten kan hebben, als kernonderdelen van het cortisolproducerende systeem zijn verstoord.
- Interessant genoeg zou de CT38-hypothese van Cortene hierbij kunnen aansluiten. Cortene stelde voor om een korte impuls van een CRFR2-agonist te gebruiken om de HPA-as te resetten. Het idee is dat chronische activering van de CRFR2-receptoren de HPA-as zou kunnen onderdrukken, waardoor de cortisolproductie wordt afgeremd. Opmerkelijk is dat een chronisch geactiveerd CRF-systeem ook zou kunnen bijdragen aan de hyperactiviteit die recentelijk in de locus caeruleus is waargenomen.
- Interessant is dat het CT38-medicijn van Cortene, als het effectief blijkt te zijn, zou kunnen helpen door de HPA-as te resetten en de druk op de hypothalamus te verlichten.
- De autopsiegegevens – die mogelijk afkomstig zijn van zeer ernstig zieke patiënten – zouden ook kunnen passen in een beeld waarin chronische neuro-inflammatie in de limbische gebieden, de PVK en de hersenstam geleidelijk de belangrijkste stressregulerende gebieden daar aantast. In dit scenario worden de NA-producerende neuronen in de locus caeruleus, de CRH-producerende neuronen in de hypothalamus en de bijnieren allemaal aangetast, en worden de twee belangrijkste stressreactiesystemen (HPA-as, autonoom zenuwstelsel) lamgelegd.
- Behandelingen om neuro-inflammatie te temperen, het immuunsysteem te kalmeren en de gevaarreactie uit te schakelen, zouden kunnen helpen.
- We kunnen meer verwachten van het Nederlandse onderzoek en het RECOVER-project van det NIH, dat – let op – al meer dan 250 longcovidpatiënten in zijn autopsiebank heeft en van plan is er ongeveer 350 op te nemen. De leermogelijkheden zijn enorm.
Wat kwam de presentatie van dr. Da Silva over “Het in kaart brengen van klinische fenotypes en disfunctie van de HPA-as bij ME/cvs” op de IACFS/ME-conferentie van 2025 toch op het juiste moment. Jose Philipe Da Silva is een neurowetenschapper verbonden aan de Universiteit van Amsterdam. We hebben zojuist gehoord van een reeks onderzoeken die de vinger rechtstreeks naar de hersenen wezen, en nu hebben we een autopsierapport over de hersenen bij ME/cvs. (Met dank aan de IACFS/ME voor hun ondersteuning bij het virtueel bijwonen van de conferentie.)

Bedenk eens: Nederland heeft gedaan wat de VS niet lukt – het is (in 2024) gestart met een hersendonatieprogramma voor ME/cvs en dat levert nu resultaten op. De NIH-Neurobank is een enorm hersendonatieprogramma dat ook ME/cvs omvat. Ze waren verbaasd over de belangstelling van ME/cvs-patiënten en beschikken vermoedelijk over enkele ME/cvs-hersenen, maar of en wat er daarmee is gebeurd, weten we niet. )
Lees ook:
Ondertussen hebben we de Nederlandse Breinbank (NBB), een gerenommeerde breinbank die bekendstaat om het leveren van hoogwaardige, vers geoogste (vreselijk woord) hersenen voor onderzoek. Volgens de website van de NBB vragen onderzoekers wereldwijd elk jaar hersenweefsel aan bij de NBB.
Deze hersenstudies geven ons een uniek inkijkje (oeps, daar ging ik weer) in ME/cvs. Tot nu toe zijn er autopsies uitgevoerd op 7 ME/cvs-donoren en er zullen er nog meer volgen. Van elke persoon was de diagnose gesteld door een ME/cvs-specialist, en de resultaten werden vergeleken met een overeenkomstige controlegroep die geen ME/cvs had.
Het is bijna zeven jaar geleden dat Health Rising voor het laatst verslag deed van autopsierapporten inzake ME/cvs. Een terugkerend thema was spinale ganglionitis – schade aan de neuronen die sensorische signalen naar het ruggenmerg doorgeven.
Lees ook:
In dit rapport werd een ander deel van de hersenen onderzocht en werd iets even interessants ontdekt.
Aandacht voor de hypothalamus-hypofyse-bijnieras (HPA-as)
Bij eerdere hersenautopsies lag de nadruk vooral op de hersenstam, maar deze groep, die gespecialiseerd is in de hypothalamus, begon bij de HPA-as, die vrijwel vanaf het allereerste begin een speerpunt is geweest in het onderzoek naar ME/cvs. Waarom? Omdat de HPA-as het belangrijkste systeem in het lichaam is voor de reactie op stress en de regulering van energie.
De hypothalamus, gelegen aan de onderkant van de hersenen, detecteert stress, bloedsuikerspiegels, ontstekingen, het tijdstip van de dag en nog veel meer. Hij zorgt voor de afgifte van corticotrofine-‘releasing’ hormoon (CRH) naar de hypofyse, die zich net onder de hersenen bevindt en vervolgens ACTH in de bloedbaan vrijgeeft. ACTH reist via de bloedbaan helemaal naar de bijnieren (bovenop de nieren).
Het eindresultaat is de productie van cortisol, dat wel de ‘stress- en energiemanager’ van ons lichaam wordt genoemd. Cortisol zorgt voor de aanmaak van energie door de bloedsuikerspiegel te verhogen en helpt ons vet en eiwitten te gebruiken bij het ontwaken en tijdens stressvolle periodes.
Het helpt ons alert en geconcentreerd te blijven en in staat te reageren op bedreigingen of uitdagingen. Het is ook een belangrijke ontstekingsremmer, helpt bij het vernauwen van bloedvaten en beïnvloedt het geheugen, de aandacht, de motivatie en de stemming.
Studies hebben aangetoond dat de cortisolspiegels in het speeksel ‘s ochtends laag zijn bij ME/cvs. Het grote longcovidonderzoek van Akiko Iwasaki leverde de nogal schokkende bevinding op dat precies een laag cortisolgehalte, eerder dan T- of B-cellen of een auto-immuunproces, een “sterke voorspellende” factor was voor long covid.
Lees ook:
Dat kwam toch wel als een verrassing. Hoewel er bij ME/cvs al onderzoek werd gedaan naar de HPA-as, denk ik niet dat iemand had verwacht dat een laag cortisolgehalte zo’n sterke voorspellende waarde zou hebben. Door de steeds grotere complexiteit van deze onderzoeken en de gebruikte technieken voor gegevensanalyse is de kans groot dat er nieuwe inzichten naar voren komen. (De groep van Iwasaki kreeg kritiek op de manier waarop ze de eerste cortisoltests hadden uitgevoerd, maar ze hebben deze herhaald en kwamen tot hetzelfde resultaat.)
De Nederlandse groep telde de neuronen in de hypothalamus, voerde een genexpressieanalyse van de hypofyse uit en bepaalde de cortisolspiegels. Gezien de lagere cortisolspiegels verwachtten ze een toename van het aantal neuronen in de hypothalamus te zien, om zo de productie van CRH omhoog te krijgen. Alles leek vrij eenvoudig, dachten ze.
CRH-productie – De hypothalamus detecteert cortisolspiegels in de bloedbaan via glucocorticoïdereceptoren (GR), die zich aan het cortisol binden. Als er te weinig GR’s worden geactiveerd, wordt de rem op de cortisolproductie opgeheven en produceert de hypothalamus meer CRH. Gezien de lage cortisolspiegels bij ME/cvs was het logisch dat de hypothalamus zou proberen dit te compenseren door meer CRH-producerende neuronen aan te maken.
Verrassing!
Alleen was dit bij de ME/cvs-patiënten niet het geval. Er was iets heel anders aan de hand. In plaats van meer CRH-producerende neuronen, vonden ze bijna geen CRH-producerende neuronen bij de ME/cvs-patiënten. Een afbeelding (onder embargo) toonde wat feitelijk een leeg scherm was met een paar vage krassen (de CRH-producerende neuronen). Daarom was het niet verrassend om drastisch lagere CRH-niveaus te zien in de vezels die naar de hypofyse lopen.
Dat wees erop dat er sprake was van een algehele onderdrukking van de hypothalamus, maar toen stonden ze weer voor een raadsel. De vasopressine- en oxytocineneuronen in de hypothalamus bleken ofwel in aantal te zijn toegenomen, ofwel op een normaal niveau te zitten. Alleen de CRH-producerende neuronen waren getroffen…
Toen ze de HPA-as verder onderzochten, troffen ze vrijwel hetzelfde aan. Uit een genexpressieanalyse bleek dat de receptoren in de hypofyse die reageren op neuropeptiden, neerwaarts waren gereguleerd.
De hypofyse reageert op tal van neuropeptiden (CRH (corticotrofine-vrijmakend hormoon), AVP (vasopressine), TRH (thyrotropine-vrijmakend hormoon), GnRH (gonadotropine-vrijmakend hormoon), GHRH (groeihormoon-vrijmakend hormoon), somatostatine en dopamine (afkomstig uit de hypothalamus)). De productie van POMC, een ‘moeder’-peptide of prohormoon dat wordt afgebroken tot ACTH, was eveneens neerwaarts gereguleerd. Tientallen jaren geleden bleek uit ME/cvs-onderzoek dat de hypofyse bij ME/cvs niet correct reageerde op CRH.
Merk op dat lage CRH-spiegels meer dan alleen cortisol kunnen beïnvloeden. Lage CRH-spiegels kunnen ook de opwinding en ‘stressbereidheid’ beïnvloeden, gevoelens van ‘onrust maar zwakte’ veroorzaken via een disfunctie van het autonome zenuwstelsel, pijn versterken, darmproblemen en slaapstoornissen veroorzaken en zo meer. Verminderde activiteit van de hypofysereceptoren kan leiden tot toegenomen pijn, verminderd libido, verhoogde gevoeligheid voor kou, enz.
Al bij al leek de HPA-as bij deze autopsiepatiënten zowat een wrak te zijn, met een drastische afname van CRH-producerende neuronen in de hypothalamus, een uitval van de hypofyse en lagere cortisolspiegels.
Aangezien het uiteindelijke doel van deze behoorlijk beschadigde HPA-as het produceren van cortisol is, zochten de onderzoekers naar aanwijzingen voor cortisolonderdrukking, en die vonden ze. Ze zijn nu op zoek naar aanwijzingen voor lage cortisolspiegels in het plasma.
Merk op dat dit mogelijk een zeer ernstig eindstadium van ME/cvs vertegenwoordigt, dat er slechts zeven autopsies zijn uitgevoerd en dat er bij personen met een mildere ziekte mogelijk meer werkzame CRH-neuronen overblijven.
Weer terug naar de toekomst?
De spreker merkte op dat lage cortisolspiegels veel van de kernsymptomen (vermoeidheid, slaapstoornissen, enz.) die bij ME/cvs worden gevonden, ten minste gedeeltelijk kunnen verklaren. We lijken dus weer bij de HPA-as uit te komen.
Da Silva deed geen uitspraken over de oorzaak. Hoewel deze bevinding nog niet is gepubliceerd en er slechts 7 autopsies zijn uitgevoerd, is het de moeite waard om te vragen wat de oorzaak zou kunnen zijn van deze vreemde disfunctie van de HPA-as en of dit aansluit bij wat we verder weten over ME/cvs? En wat zouden de mogelijke hypofyseproblemen kunnen veroorzaken?
Ten eerste moet worden opgemerkt dat de hypothalamus in de loop der tijd veel belangstelling heeft getrokken. In 2014 concentreerde Dr. Bateman zich op inflammatie in de thalamus, hypothalamus en hypofyse. In 2018 stelde Theoharides dat mestcellen in de hypothalamus neuro-inflammatoire stoffen uitstoten die de bloed-hersenbarrière openen, de mitochondriën beschadigen en tegelijkertijd neuro-inflammatie veroorzaken.
In 2020 veronderstelde Angus Mackay op nogal sinistere wijze – aan de hand van een gedachte-experiment – dat de ‘stressintegrator’ in de hypothalamus, de paraventriculaire kern (PVK) genaamd, mogelijk een sleutelrol speelt bij ME/cvs. De PVK blijkt de belangrijkste producent van CRH te zijn.
Lees ook:
A Novel Neuroinflammatory Paradigm for Chronic Fatigue Syndrome (ME/CFS)
Mackay stelde dat een ontstoken PVK mogelijk te veel CRH aanmaakt. Hoewel uit dit onderzoek bleek dat er sprake was van een laag aantal CRH-producerende neuronen, zou het scenario van Mackay, waarin de PVK hyperactief is, kunnen leiden tot schade op de lange termijn en het mogelijk verdwijnen van die neuronen.
De situatie komt maar al te bekend voor: het is weer een nieuwe variant op het probleem van ‘opgedraaid en uitgeput’ / ‘opgebrand’ maar vastzitten in de alarmmodus, dat bij deze aandoeningen veel lijkt voor te komen.
Maar waarom zouden alleen CRH-producerende neuronen in de hypothalamus aangetast zijn? Misschien omdat vasopressine- en oxytocine-producerende neuronen zich, althans gedeeltelijk, in andere delen van de PVK bevinden. Er zijn verschillende hypothesen geponeerd met betrekking tot bijnierdisfunctie, maar in dit scenario zou de bijnierfunctie verstoord kunnen zijn omdat de bijnieren ‘onderbelast’ zijn.
Het mag niet onopgemerkt blijven dat de recente (nog niet gepubliceerde) bevinding over noradrenaline (NA) hiermee verband zou kunnen houden. Dichte strengen van noradrenerge (noradrenaline-producerende) vezels komen vanuit de locus caeruleus rechtstreeks in de PVK terecht, waar ze de productie van CRH op gang brengen. De hyperstimulatie in de NA-neuronen zou hyperactieve CRH-neuronen in de hypothalamus kunnen veroorzaken, die uiteindelijk uitgeput raken.
Lees ook:
Deze bevindingen geven aan waarom het toedienen van cortisol in de vorm van een lage dosis hydrocortisone soms negatieve effecten kan hebben, als cruciale delen van het cortisolproducerende systeem niet goed functioneren.
Het is interessant dat de CT38-hypothese van Cortene hierin zou kunnen passen. Cortene stelde voor om een korte puls van een CRFR2-agonist (Corticotropin-Releasing Factor Receptor type 2) te gebruiken om de HPA-as te resetten. Het idee is dat chronische activering van de CRFR2-receptoren de HPA-as zou kunnen onderdrukken, waardoor de cortisolproductie wordt gedempt. Interessant is dat een chronisch geactiveerd CRF-systeem ook zou kunnen bijdragen aan de hyperactiviteit die recentelijk is waargenomen in de locus caeruleus.*
Lees ook:
The Cortene Drug Trial Results for ME/CFS Are In
De autopsiegegevens – die mogelijk afkomstig zijn van zeer ernstig zieke patiënten – zouden ook kunnen passen in een scenario waarin chronische neuro-inflammatie in de limbische gebieden, de PVK en de hersenstam langzaam de belangrijkste stressregulerende gebieden daar aantast. In dit scenario worden de NA-producerende neuronen in de locus caeruleus, de CRH-producerende neuronen in de hypothalamus, en de bijnieren allemaal getroffen, en worden de twee belangrijkste reactiesystemen op stress (HPA-as, autonoom zenuwstelsel) lamgeslagen. De situatie bereikt een dieptepunt als uitgeputte neuronen beginnen te verdwijnen.
Uit het onderzoek bleek dat enkele neuronen overbleven, en het is mogelijk dat andere te gekrompen waren om zichtbaar te zijn. Hoewel neuronregeneratie in het centrale zenuwstelsel kan optreden, is dit beperkt. Inflammatie verminderen, de stressrespons afremmen en CT38 gebruiken om de HPA-as te resetten, zou in theorie een aanzienlijke compensatie kunnen bieden.
Behandeling?
Het lijkt wel alsof we altijd weer op inflammatie uitkomen, wat eigenlijk goed nieuws is, want het bestrijden van ontstekingen is een enorm belangrijk onderwerp in de medische wereld. Als neuro-inflammatie de oorzaak is van deze verstoring van de HPA-as, zouden verschillende behandelmethoden kunnen helpen.
Op dit moment beschikken we blijkbaar niet over echt krachtige middelen tegen neuro-inflammatie, maar een aantal behandelingen (minocycline, GLP-1-agonisten, mestcelstabilisatoren, laaggedoseerde naltrexone, PEA, stimulatie van de nervus vagus, cytokineblokkers zoals etanercept) zouden daarbij kunnen helpen. De effecten van ibudilast, NLRP3-remmers, CNS BTK-remmers en TREM2-agonisten op neuro-inflammatie worden momenteel onderzocht. Door de prefrontale cortex te activeren, zou rTMS de neuronen in de locus caeruleus kunnen ontlasten. Baricitinib en andere JAK-remmers (bijv. REVERSE-LC) en geneesmiddelen zoals bezisterim kunnen onrechtstreeks helpen door de afweerreactie te kalmeren.
Neuroplasticiteitsoefeningen kunnen bij sommigen de reactie op gevaar mogelijk afzwakken, waardoor het systeem zich kan resetten. Ik heb berichten gehoord dat de Suramin-studie van Bob Naviaux om de reactie op gevaar uit te schakelen, mogelijk op gang komt.
We hebben een aantal veelbelovende berichten ontvangen van de IACFS/ME-conferentie die goed op elkaar lijken aan te sluiten. Let wel: we wachten nog steeds op de publicatie van deze onderzoeken, en het Nederlandse onderzoek was vrij kleinschalig – dus de tijd zal het leren. We zullen waarschijnlijk meer van hen horen naarmate ze meer patiënten onderzoeken en meer delen van de hersenen in kaart brengen.
De grote olifant in de autopsiekamer is het RECOVER-initiatief, dat al – let wel – meer dan 250 longcovidpatiënten heeft gekregen voor autopsie en van plan is van nog eens ongeveer 350 autopsies te doen.
*Ik ben lid van het bestuur van Cortene.
Video over het onderwerp:
© Cort Johnson, Health Rising, 4 december 2025. Vertaling Els, ME-gids.





