De kernpunten
- Over zaken die in de lucht hangen gesproken. Net toen David Goldstein op de IACFS/ME-conferentie bewijs leverde dat de productie van noradrenaline in de hersenen bij ME/cvs sterk was afgenomen en dat het sympathisch zenuwstelsel zwak en ondermaats functioneerde, kwamen neurowetenschapper Jolien Hendrix en haar collega’s in België tot de conclusie dat hetzelfde gebeurde, niet in de hersenen, maar in het lichaam.
- De algemeen aanvaarde opvatting is dat bij ME/cvs het sympathisch zenuwstelsel (SZS), oftewel het ‘vecht- of vluchtsysteem’, geactiveerd is en dat het parasympathisch zenuwstelsel (PZS), oftewel het ‘rust- en verteringssysteem’, gedempt is. Dat is logisch gezien het ‘opgedraaid maar uitgeput’-fenomeen, dat lijkt aan te geven dat vechten/vluchten op volle toeren draait, terwijl het ‘rust- en verteringssysteem’, dat ons helpt te herstellen, grotendeels uitgeschakeld is.
- Toen deze onderzoekers echter keken naar wat er tijdens en na lichaamsinspanning met het sympathisch zenuwstelsel gebeurde, ontdekten ze iets anders. Bij gezonde personen treedt het sympathisch zenuwstelsel in werking om bloed en voedingsstoffen naar de spieren te brengen. Bij ME/cvs-patiënten wordt het echter niet geactiveerd, maar juist afgeremd.
- Waarom zou het SZS zichzelf uitschakelen juist wanneer het echt nodig is? Waarschijnlijk om zichzelf te beschermen. Het blijkt dat de vecht- of vluchtreactie inderdaad in overdrive is, maar dan wel continu. De auteurs vermoeden dat het systeem al zo uitgeput is dat, wanneer het tijd is om de motoren te starten, het gas terugneemt om te voorkomen dat het (bij wijze van spreken) een zekering doorbrandt. We hebben dit patroon keer op keer gezien in studies naar lichaamsinspanning.
- Dit lijkt heel goed te passen bij het concept van Bob Naviaux dat het lichaam van ME/cvs-patiënten zich in een toestand van ‘celgevaarreactie’ bevindt en zich als het ware terugtrekt om schade te voorkomen.
- De lage noradrenaline (NA)-niveaus in de hersenen, van Goldstein/Aregawi wat we onlangs hebben besproken, lijken heel goed bij deze bevindingen aan te sluiten. Omdat de belangrijkste producent van NA in de hersenen, de locus caeruleus, een sterke band heeft met de neuronen van het sympathisch zenuwstelsel, zou een verminderde productie in de hersenen kunnen leiden tot een compenserende inspanning van het lichaam om de activiteit van het sympathisch zenuwstelsel te stimuleren.
- Na verloop van tijd zou die chronische activering ook het SZS in het lichaam kunnen uitputten. Uiteindelijk krijgen we dan twee vecht-/vluchtsystemen – één in de hersenen en één in het lichaam – die beide verzwakt en uitgeput zijn geraakt.
- Omdat het sympathisch zenuwstelsel de reactie op lichaamsbeweging coördineert, is het mogelijk dat deze vreemde uitputting zich vertaalt in de vele storingen op moleculair niveau om al dan niet of niet goed te reageren op lichaamsbeweging, zoals de Hanson-groep heeft vastgesteld.
- Er lijken veel overeenkomsten te zijn, maar we moeten voorzichtig zijn: dit zijn vroege studies en hun bevindingen moeten worden herhaald en verder worden onderzocht. Toch was het zeer bemoedigend om te zien dat twee onafhankelijke onderzoeksgroepen binnen een paar weken tot vrijwel dezelfde conclusie kwamen met betrekking tot het sympathisch zenuwstelsel – één in de hersenen en één in het lichaam.
Over dingen die in de lucht hangen gesproken. Net toen David Goldstein op de IACFS/ME-conferentie bewijs leverde dat de productie van noradrenaline in de hersenen bij ME/cvs sterk was afgenomen en dat het sympathisch zenuwstelsel zwak en ondermaats functioneerde, kwamen neurowetenschapper Jolien Hendrix en haar collega’s in België tot de conclusie dat hetzelfde gebeurde, niet in de hersenen maar in het lichaam.

Hendrix en haar collega’s kwamen tot deze nogal verrassende conclusie niet door een experiment, maar door een literatuuronderzoek; d.w.z. een conclusie die blijkbaar voor het grijpen lag. Het eerste systematische onderzoek naar ‘biologisch bewijs van adrenerge disfunctie bij patiënten met ME/cvs en FM’ was inderdaad een openbaring. (Met maar liefst vijf publicaties over ME/cvs of long covid in het afgelopen jaar en nog meer publicaties over chronische pijn zijn deze Belgische onderzoekers zeer actief geweest.)
Hun recente artikel, “Adrenergic dysfunction in patients with myalgic encephalomyelitis/chronic fatigue syndrome and fibromyalgia: A systematic review and meta-analysis“ [Adrenerge disfunctie bij patiënten met myalgische encefalomyelitis/chronischevermoeidheidssyndroom en fibromyalgie: een systematische review en meta-analyse], biedt een mooie onderbouwing voor de conclusie van Goldstein en Aregawi.
Opmerking: wanneer u het woord ‘adrenergisch’ ziet, denk dan aan het sympathisch zenuwstelsel. Het woord adrenergisch verwijst naar adrenaline, dat tegenwoordig meestal epinefrine (nvdr: in het Engels taalgebied) wordt genoemd. (Adrenergisch is afgeleid van een Grieks woord dat ‘wegjagen’ betekent.)
De hersenen en het lichaam?
De auteurs kwamen meteen ter zake door te melden dat eerdere reviews “consequent de sympathische dominantie bij ME/cvs hadden benadrukt, wat blijkt uit een verhoogde hartslag en verminderde hartslagvariabiliteit”. De nieuwe review bracht meer bewijs aan het licht voor de dominantie van het sympathisch zenuwstelsel (verhoogde adrenaline- (noradrenaline-) niveaus en verhoogde B1AR-expressie op baseline)
De consensus was inderdaad dat het sympathisch zenuwstelsel (SZS), of “vecht- of vluchtsysteem”, was geactiveerd en dat het parasympathisch zenuwstelsel (PZS), of “rust- en verteringssysteem”, was onderdrukt bij ME/cvs. Omdat het PZS het SZS reguleert, is het idee om het PZS te versterken zodat het SZS kalmeert en het lichaam kan rusten en herstellen.
Maar toen deze onderzoekers keken naar wat er na inspanning gebeurde, veranderde er iets. ME/cvs-patiënten vertoonden een grotere stijging in verschillende adrenerge receptoren (α₂A AR, β2 AR en COMT) en in de expressie van het COMT-gen dan gezonde controlegroepen.

(Door hun interactie met de externe omgeving bepalen de receptoren op een cel wat de cel doet; d.w.z. de activering van een receptor zet de cel aan tot een bepaalde handeling. De cel maakt bepaalde handelingen waarschijnlijker door het aantal receptoren aan de buitenkant te vermeerderen. De verhoogde aantallen van deze adrenerge receptoren na inspanning vergroten de kans op activiteit van het sympathisch zenuwstelsel. De vraag is: wat voor soort activiteit?
In dit geval remmen de α₂A AR-receptoren de afgifte van catecholamines (noradrenaline, adrenaline en dopamine) en COMT werkt als katalysator voor de afbraak van catecholamines.
Lichaamsbeweging lijkt dus het niveau van de neurotransmitters die het sympathisch zenuwstelsel aansturen, te verlagen. De auteurs zijn van mening dat de cellen bij ME/cvs het sympathisch zenuwstelsel (SZS) (net op het verkeerde moment) afremmen omdat het al overactief was (bijv. verhoogde hartslag, verminderde hartslagvariabiliteit, verhoogde adrenaline (epinefrine) en B1AR-expressie op basisniveau) vóór de lichaamsbeweging.
Merk op dat bij gezonde personen het tegenovergestelde gebeurt: lichaamsbeweging veroorzaakt een tijdelijke toename van catecholamines en activiteit van het sympathisch zenuwstelsel om zuurstof en voedingsstoffen naar de spieren te brengen.

Als deze onderzoekers gelijk hebben, dan is het niet verwonderlijk dat ME/cvs- patiënten moeite hebben met sporten: terwijl gezonde mensen hun SZS juist stimuleren om te kunnen sporten, schakelen ME/cvs-patiënten hun SZS juist uit.
Het SZS lijkt zelfs in tegenspraak met zichzelf te zijn. Terwijl het SZS wordt afgeremd, neemt de B2 AR-expressie, mogelijk als compensatie, toe om zo veel mogelijk profijt te halen uit de aanwezige catecholamines.
De bevindingen suggereren dat ME/cvs een noradrenalinesysteem met een hoge stimulering en een lage capaciteit kan zijn; d.w.z. dat het gaspedaal in het SZS volledig wordt ingedrukt, maar dat de motor snel vastloopt – iets wat we keer op keer hebben gezien bij inspanningsonderzoeken.
Hypothese
Op dit moment is dit een hypothese en de auteurs erkennen dat er nog meer onderzoek nodig is om ze goed te kunnen toetsen. Ze hebben een mechanistisch pad ontworpen om dat te doen, dat catecholaminemetabolieten, enzymen die betrokken zijn bij de catecholaminesynthese, en genetische/epigenetische factoren omvat.
Zij zijn van mening dat de subgroep met hyperadrenerge POTS-neiging soms te maken kan hebben met een enorme toename van noradrenaline en mogelijk meer compenserende opwaartse regulering van de remmende factoren (α₂A/COMT). Die groep zou in studies moeten worden uitgesplitst.
De bevindingen over hersenen integreren
Hendrix et al. waren duidelijk niet op de hoogte van de nog niet gepubliceerde bevinding van Goldstein/Aregawi, die wees op een lage productie van noradrenaline in de hersenen. Die groep kwam tot deze conclusie door metabolieten te meten – een van de elementen die volgens Hendrix et al. ontbraken.
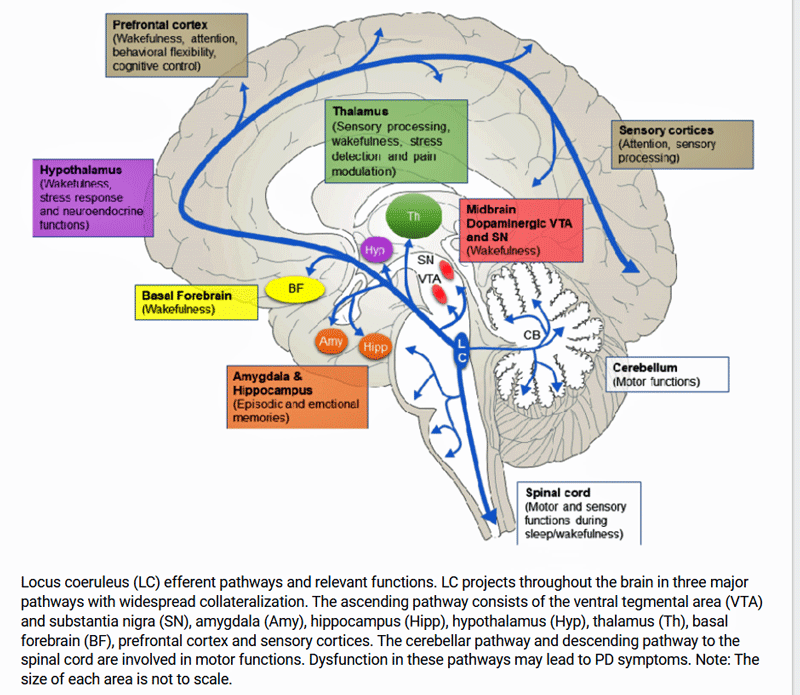
De lage noradrenalineniveaus in de hersenen van Goldstein/Aregawi komen mogelijk goed overeen met de bevindingen van Hendrix et al. De belangrijkste producent van noradrenaline in de hersenen – de locus caeruleus – heeft sterke verbindingen met neuronen van het sympathisch zenuwstelsel en de hypothalamus en hersenstam. (Merk op dat de recente (niet-gepubliceerde) autopsieresultaten ook de hypothalamus noemden.
De ‘vervuilde signalen’ die afkomstig zijn van de locus caeruleus, veroorzaken storingen in het autonome zenuwstelsel en activeren dit op misschien wel de slechtst mogelijke manier: omdat het systeem niet weet welke kant het op moet, blijft het in een staat van constante waakzaamheid. Dit leidt tot pijn, vermoeidheid en orthostatische intolerantie.
Uiteindelijk doet zich in beide gevallen hetzelfde probleem voor (een overbelast, uitgeput SZS). In dit scenario wordt het proces waarschijnlijk in gang gezet door een verminderde noradrenalineproductie in de hersenen. Na verloop van tijd besluit een chronisch geactiveerd SZS-systeem in het lichaam dat het genoeg is geweest en zet het zich tijdens inspanning bij ME/cvs automatisch uit om schade te voorkomen. De systemen die op inspanning kunnen reageren, doen dat vaak op een pathologische manier.
Dit lijkt goed aan te sluiten bij het idee van Naviaux dat een “celgevaarreactie” het lichaam in een soort beschermende, winterslaapachtige toestand houdt.
Merk op dat de (niet-gepubliceerde) autopsieonderzoeken ook wijzen op de aanwezigheid van een overbelaste, uitgeputte hypothalamus en HPA-as.
De bevindingen inzake gebrek aan reactie
De bevindingen van de Hanson-groep suggereren dat op moleculair niveau veel systemen (metabolieten, proteomica, genexpressie) niet reageren (urinaire metabolieten, extracellulaire vesikels, genexpressie) of pathologisch reageren (plasma-metabolomica, proteomica) op lichaamsbeweging. Het is mogelijk dat het sympathisch zenuwstelsel niet in staat is om op de situatie te reageren en een gecoördineerde reactie op lichaamsbeweging te geven.
Het idee dat fundamentele systemen zoals de HPA-as (zie autopsieblog) en het sympathisch zenuwstelsel in een uitgeputte maar gespannen toestand verkeren, is behoorlijk overtuigend. We zouden immers verwachten dat centrale systemen volledig in de war moeten zijn geraakt om het soort functionele schade te veroorzaken dat bij deze ziekten optreedt.
Dit alles moet worden getest. Hopelijk zijn er voldoende gegevens gerapporteerd zodat onderzoeksgroepen dit gaan onderzoeken. We hebben studies nodig die al deze gegevens omvatten – de bevindingen over noradrenaline in het hersenvocht, hersenscans, adrenerge bevindingen in het lichaam en multi-omica-bevindingen voor en na het sporten – om te bepalen of dit scenario klopt.
De tijd zal het uitwijzen. In de tussentijd lijken de verbanden zich op te stapelen.
© Health Rising, 7 december 2025. Vertaling Els, redactie admin, ME-gids.
Citeren?
Hendrix, J., Fanning, L., Wyns, A., Ahmed, I., Patil, M. S., Richter, E., Van Campenhout, J., Ickmans, K., Mertens, R., Nijs, J., Godderis, L., & Polli, A. (2025). Adrenergic dysfunction in patients with myalgic encephalomyelitis/chronic fatigue syndrome and fibromyalgia: A systematic review and meta-analysis. European journal of clinical investigation, 55(1), e14318. https://doi.org/10.1111/eci.14318





