 Cort Johnson, Health Rising, 11 juli 2020
Cort Johnson, Health Rising, 11 juli 2020
Travis Craddock leidde het project. © Facebook Nova Southeastern University Institute for Neuro Immune Medicine
Travis Craddock staat aan het hoofd van Dr. Klimas’ bio-informaticamodelleerteam aan het Instituut voor Neuro-Immunologische Geneeskunde (INIM) van de Nova Southeastern University. Dit is het team dat verantwoordelijk is voor het uitpluizen van de honderdduizenden meetgegevens uit Dr. Klimas’ intensieve inspanningsstudies tot een gigantisch model van hoe het immuunsysteem, het neuro-endocriene systeem en andere systemen in het lichaam met elkaar interageren.
Er is een heel dorp voor nodig – een onderzoeksgroep van bio-informatica-experts – en in dit geval, ook een supercomputer. Het was dit team en hun werk dat Dr. Klimas gebruikte om reusachtige subsidies voor Gulf War Illness (GWI, Golfoorlogsyndroom) in de wacht te slepen en een aantal nieuwe klinische studies te ontwerpen.
Het onderzoek was op verschillende vlakken apart. Het team dook met het hoofd eerst in een stapel genetische gegevens en kwam weer boven met iets totaal onverwachts. Iets wat je met andere ogen naar deze ziekte kan doen kijken.
En Craddock et al. hebben geen dataset gebruikt met een productiekost van 100.000 dollar. De genetische gegevens die deze verrassingsvondst opleverden, waren een gulle gift van de ME/cvs-gemeenschap.
“The Great Chronic Fatigue Syndrome Community Gene Study” die de gegevens produceerde (bekend bij hen die ze creëerden als de “ME/CFS Genetic Database Study”), bestond volledig uit genetische informatie die werd verstrekt door patiënten uit hun 23andMe- of Ancestry.com-datasets. Ze was het resultaat van een communityproject dat door het team van Dr. Klimas werd gelanceerd.
Craddock sprak over zijn prille resultaten rond 1 uur en 55 minuten in het recente 3 uur durende webinar van INIM.
https://www.youtube.com/watch?v=QfrCF2atQxI
INIM Webinar – Understanding ME/CFS Today: A Clinical & Research Approach
INIM Webinar – Understanding ME/CFS Today: A Clinical & Research Approach Speakers: 1. (0:08:17) Maria Vera-Nunez, M.D., MSBI, DABOIM, IFMCP – Physician An I…
Voel je je slijmerig?
De studie had al bewijs gevonden van een erfelijk defect in het methylfolaatgen (MTHFR) bij ME/cvs. Dat was niet geheel onverwacht, maar niemand voorzag de plakkerige situatie die in de meest recente analyse opdook.
Een opmerkelijk groot deel (77-80%) van de personen met ME/cvs bleek veranderingen te hebben in de genen die een slijmlaag produceren. Ja, slijm. Kleverig, plakkerig, smerig slijm – in wetenschappelijke termen, een “complexe, verdunde waterige visco-elastische secretie” of “viskeuze gel” – ook wel bekend als slijm. Slijm krijgt over het algemeen niet veel respect, maar het speelt eigenlijk een cruciale rol in onze gezondheid.
Slijm bekleedt onze neus, onze luchtwegen, onze darmen, onze ogen. Het werpt een vitale barrière op tegen chemicaliën, virussen en schimmels en houdt ze vast. Het beschermt ook tegen uitdroging, lichamelijk letsel, enz. Het bevat ook immuunfactoren om vervelende ziekteverwekkers te bestrijden of giftige stoffen op te ruimen. Zonder onze beschermende slijmvliesbarrières zou ons lichaam overspoeld worden door giftige of ziekmakende stoffen.
Er zitten meer dan 100 eiwitten in het slijmvlies, waardoor de concentratie van mutaties die Craddock vond bij ME/cvs – allemaal in de genen die MUC19 van het slijm produceren – opmerkelijk te noemen is.

Een van de genetische afwijkingen die Craddock vond, was inderdaad opmerkelijk.
Kleine afwijkingen in deze genen zijn voorlopig in verband gebracht met het syndroom van Sjögren – die volgens sommigen een dramatisch ondergediagnosticeerde ziekte is bij het posturaal orthostatisch tachycardiesyndroom (POTS) en aanverwante aandoeningen – en ook met de ziekte van Crohn en astma.
Er zijn mutaties in genen en er zijn ook MUTATIES. De meeste kleine genetische afwijkingen maken weinig of geen verschil. Andere veranderen drastisch de werking van het eiwit dat ze aanmaken. Een van de genetische afwijkingen viel in de laatste categorie. Ze was nagenoeg net zo schadelijk als een genetische mutatie kan worden: mensen met dit gen (ik zou niet kunnen zeggen welk percentage van de patiënten deze had) maken een schamel, afgekapt, waarschijnlijk volledig disfunctioneel eiwit aan, dat een derde van de normale grootte is.
Terug naar Baraniuk
Dit is overigens niet de eerste keer dat ME/cvs-onderzoekers rond gesnuffeld hebben aan de neus. Ongeveer tien jaar geleden heeft James Baraniuk jaren lang afgetast, uitgeplozen en geprobeerd te begrijpen wat er in de nasale doorgangen van mensen met ME/cvs gebeurde.
https://www.healthrising.org/blog/2019/10/14/phantom-nasal-congestion-chronic-fatigue-fibromyalgia/
What “Phantom Nasal Congestion” May Tell Us About ME/CFS and Fibromyalgia – Health Rising
When you have a systemic disease, any part of your body can provide a clue – even your nose. Over 15 years from 1998 to 2012, James Baraniuk, a longtime ME/CFS and GWI researcher at Georgetown University, became the first and thus far the last person to try and understand people with fibromyalgia or chronic fatigue syndrome (ME/CFS) through their nose.
Baraniuk vond dat pijn aan de sinussen en niet-allergische rinitis bij een aanzienlijk aantal mensen met ME/cvs voorkomen. In feite waren de regio’s in het midden van het gezicht bij mensen met ME/cvs pijnlijker dan bij mensen met gedocumenteerde lichamelijke afwijkingen, zoals allergische rinitis of rinosinusitis.
Vaak worden de symptomen van middenaangezichtspijn (druk op de neus, zwaarte, spanning, blokkering van de neus) mogelijk aangezien voor spanningshoofdpijn. De pijn is over het algemeen symmetrisch, treft beide zijden van het gezicht en heeft meestal geen duidelijke verergerende factoren. Pijnstillers, antibiotica en intranasale steroïden zijn meestal niet effectief.
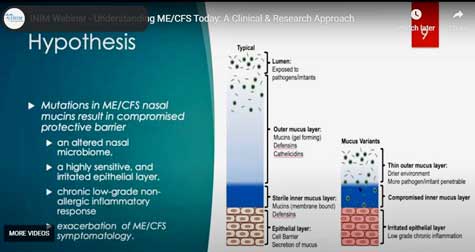
De waargenomen afwijkingen aan het slijmvlies werden in de buitenste gellaag gevonden. © INIM Webinar.
Baraniuk was niet in staat om een bewijs te vinden van zwelling of blokkades in de neus van ME/cvs-patiënten die de gevoelens van pijn, zwaarte en congestie, die ze doorgaans ondervonden, zouden kunnen verklaren. Noch slaagde hij erin om tekenen van ontsteking (totaal eiwit, NGF, TNF-a, IL-8), mestcelactivering of een allergische reactie (verhoogde IgE-niveaus) te vinden die zouden kunnen verklaren waarom het middelste gedeelte van hun gezicht zo gevoelig was.
Baraniuk kwam tot de conclusie dat de meeste mensen met deze ziektes leden aan iets wat idiopathische niet-allergische rinitis (iNAR) wordt genoemd.
Verband met dunnevezelpolyneuropathie (DVPN)?
Acht jaar geleden, lang voordat het DVPN-nieuws bij FM de aandacht trok, beweerde Dr. Baraniuk dat de schade aan precies deze dunne zenuwvezels (type C-neuronen) de oorzaak was van de middenaangezichtspijn die hij aantrof bij ME/cvs.
Hij suggereerde dat hyperactieve (TRPV1) ionenkanalen op de zenuwen in de neus een niet-aflatende stroom van signalen stuurden naar de hersengebieden die betrokken zijn bij de verwerking van pijn. Na verloop van tijd leidde dit tot centrale overgevoeligheid – een opwaartse regulering in de pijnproducerende signaalpaden en een neerwaartse regulering in de pijnremmende signaalpaden in de hersenen.
Uiteindelijk werd zelfs minimale sensoriële input van de neus door een centraal overgevoelig brein omgezet in gewaarwordingen van pijn, zwaar gevoel in de neus en congestie – een congestie die Baraniuk “fantoomneuscongestie” noemde – in navolging van fantoompijn bij de ledematen.
Is Fibromyalgia and Chronic Fatigue Syndrome Actually Small Fiber Polyneuropathy? – Health Rising
Chronic fatigue syndrome (ME/CFS) and fibromyalgia (FM) produce so many symptoms that diagnosing them can be difficult for uninformed doctors. While we know that small fiber polyneuropathy (SFPN) (or small fiber neuropathy (SFN) commonly occurs in both these diseases, what I didn’t realize until I read the two articles below […]
Baraniuk ging zelfs nog verder. Aangezien een bepaalde vorm van rinitis namelijk “dysautonomische rinitis” veel voorkomt bij ME/cvs, probeerde Baraniuk zelfs autonome problemen die veroorzaakt worden door de hersenstam, te koppelen aan de ontregelde verwerking van zintuiglijke informatie door de thalamus – en de neus.
Baraniuk dacht dat dezelfde soort rinitis zich voordoet bij FM, migraine, Golfoorlogsyndroom, meervoudige chemische sensitiviteit, prikkelbaredarmsyndroom en interstitiële cystitis. (Al deze ziekten, merkte hij op, ontvangen lage financiering van de NIH.)
Een genetisch verband?
Acht jaar later duiken er mutaties op in de genen die de beschermende slijmlagen produceren in de neus en op andere plaatsen.
Deze 19 eiwitten vormen de buitenste gellaag van het slijmvlies dat belet dat toxines, ziekteverwekkers en irriterende stoffen in de buurt komen van de huidlaag waar de zenuwen zich bevinden.
Craddock beweerde dat de gecompromitteerde gellaag zou kunnen leiden tot een veranderd microbioom in de neus, de neusmembranen zou kunnen irriteren en een chronische en laaggradige niet-allergische ontstekingsreactie zou kunnen veroorzaken. De bijgevolg geïrriteerde zenuwen zouden kunnen leiden tot een verhoogde gevoeligheid voor vaak voorkomende chemische stoffen.
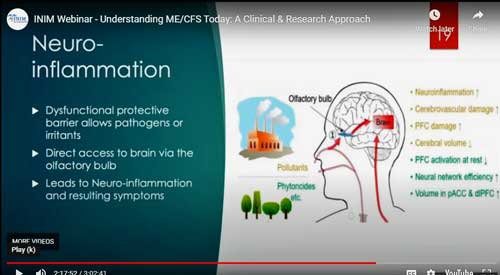
Craddock speculeerde of een disfunctionele slijmlaag zou kunnen bijdragen tot neuro-inflammatie bij ME/cvs. © INIM Webinar.
Craddock merkte op dat een verzwakte slijmlaag ziektekiemen, giftige en andere stoffen in het bloed kan laten terechtkomen (lekkendeneussyndroom?) en een systemische reactie kan uitlokken die andere ME/cvs symptomen doet opflakkeren.
Merk op dat het neusmicrobioom op dit moment een populair onderwerp is. Craddock meldde dat, net als in de darm, een gezonde microbioompopulatie in de neus een cruciale rol speelt in het behoud van de neusgezondheid. Aangezien het neusmicrobioom een afspiegeling is van het nasaal milieu, zou een gecompromitteerde slijmlaag vrijwel zeker resulteren in een veranderd neusmicrobioom. Hij vermoedde dat, als het neusmicrobioom bij ME/cvs aangetast was, misschien door een bacteriële infectie, en niet in staat was om terug te keren naar een gezonde toestand, het de neus gevoeliger zou kunnen maken voor virussen en andere pathogene en chemische stoffen.
Craddock en zijn team, duidelijk enthousiast over hun bevindingen, zijn zo ver gegaan dat ze een logisch model hebben opgesteld dat aangeeft wat er zou gebeuren als bij iemand met een gecompromitteerde slijmlaag een pathogeen door de gellaag heen zou komen. Het model leverde één gezonde situatie op (de ziekteverwekker wordt bestreden en alles wordt weer normaal) en twee ongezonde situaties – waarvan een met een aangeboren immuunsysteem dat op scherp staat en klaar is om bij de geringste prikkel in actie te komen. (Dat zou een overactivering van de NK-cellen behelzen. En dit zou op zijn beurt misschien kunnen leiden tot uitputting van de NK-cellen en de afname van de cytotoxiciteit die bij ME/cvs wordt vastgesteld).
Maar er is nog een andere mogelijkheid die als een donkere wolk opdoemt: neuro-inflammatie. Zoals Health Rising onlangs meldde in een blog over het gebruik van intranasale geneesmiddelen voor de behandeling van neuro-inflammatie en andere hersenaandoeningen, zorgt de neus voor een vrijwel directe toegang tot de hersenen. Voeg daar een beschadigde slijmvlieslaag in de neus aan toe, en een gewijzigd neusmicrobioom met een snelle weg naar de hersenen, en dan heb je misschien gevaarlijke substanties (pathogene, irriterende of giftige stoffen) die in de hersenen terechtkomen en neuro-inflammatie veroorzaken.
Het is een intrigerende hypothese die veel meer validering vereist. Craddock et al. hopen nauwkeuriger genetische analyses uit te voeren, het neusmicrobioom bij ME/cvs te onderzoeken, de samenstelling van het slijm in de neus of de tranen te analyseren en het gebruikte model te verbeteren.
De grote lijnen
- De genetische studie over ME/cvs van Nancy Klimas, die gebaseerd was op de community en erdoor werd ondersteund, leverde een verrassende bevinding op: hoge percentages van mutaties in de genen die een bepaald soort mucosaal eiwit (o.m. MUC19) produceren.
- Minstens één van deze mutaties heeft het potentieel om dat eiwit ernstig te beschadigen, waarbij het gereduceerd wordt tot een derde van zijn normale grootte.
- MUC19 is betrokken bij de productie van de gellaag die ons beschermt tegen pathogenen en toxines en die immuun- en andere factoren bevat.
- Beschadigde slijmvliezen in de ogen, de neus en de bovenste luchtwegen zouden pathogenen en toxines een eenvoudiger toegang tot het lichaam kunnen geven en misschien, gezien de rechtstreekse lijn van de neus naar de hersenen, ook naar de hersenen.
- Systemische ontsteking, neuro-inflammatie en centrale overgevoeligheid zouden allemaal denkbare gevolgen kunnen zijn.
- Ongeveer tien jaar geleden vonden de studies van Baraniuk over de neus hogere percentages van middenaangezichtspijn dan bij allergische rinitis en sinusitis. Hij was echter niet in staat om bewijs te vinden van ontsteking, mestcelactivering, schade of een andere mogelijke oorzaak.
- Baraniuk geloofde dat de dunne zenuwvezels in de neus van ME/cvs-patiënten beschadigd waren en een reeks pijnsignalen naar de hersenen stuurden – wat mogelijk de oorzaak was van of bijdroeg tot centrale overgevoeligheid.
- Craddocks ontdekking van gemuteerde genen verantwoordelijk voor de aanmaak van mucosale eiwitten in de neus, is een mogelijke verklaring voor de ontdekking van Baraniuk.
- Craddock hoopt zijn genetische studies te kunnen uitbreiden, rechtstreeks het microbioom en de slijmsamenstelling in de neus van ME/cvs patiënten te kunnen analyseren, zijn modelleringsstudies te kunnen uitbreiden, enz. om uit te maken of deze vroege bevinding klopt.
© Health Rising. Vertaling Els, redactie Zuiderzon, ME-gids.







