What about ME? is een miniserie van artikelen die op me-gids.net verscheen in aanloop naar Wereld ME Dag op 12 mei 2016. De miniserie is gericht op het belang van en het effect van (inter)nationale patiënteninbreng/acties en hun directe invloed op belangrijke ontwikkelingen rond ME.
What about ME? is een miniserie van artikelen die op me-gids.net verscheen in aanloop naar Wereld ME Dag op 12 mei 2016. De miniserie is gericht op het belang van en het effect van (inter)nationale patiënteninbreng/acties en hun directe invloed op belangrijke ontwikkelingen rond ME.
In Deel I bespraken wij de actie van ME patiënt Clark Ellis, die erop aandrong dat patiëntenorganisaties zich veel duidelijker dienden uit te spreken. Resultaat: een wereldwijde oproep van internationale patiëntenorganisaties voor het vrijgeven van de data van de PACE trial.
 In Deel II stond petitie “ME is geen SOLK” centraal. Nederlandse patiënten kwamen in actie na het bekend worden van de gezondheidsraadcommissie die de opdracht heeft een belangrijk adviesrapport te schrijven aan de Tweede Kamer over ME. Resultaat: wereldwijd is er aandacht voor deze petitie. Al vele patiënten en ook vele bekende ME experts, waaronder Dr. Weir, Dr. VanNess, Dr. van Elzakker, Dr. Zeineh, prof. Racaniello, Prof. Coyne, A. Whittemore, tekenden de petitie. Er zijn al bijna 3000 handtekeningen opgehaald. Iedere handtekening is nog steeds zeer welkom. Immers ME is geen SOLK, het biopsychosociaal model is niet van toepassing, CGT is geen behandeling. Een paradigmashift in het denken over ME is hard nodig!
In Deel II stond petitie “ME is geen SOLK” centraal. Nederlandse patiënten kwamen in actie na het bekend worden van de gezondheidsraadcommissie die de opdracht heeft een belangrijk adviesrapport te schrijven aan de Tweede Kamer over ME. Resultaat: wereldwijd is er aandacht voor deze petitie. Al vele patiënten en ook vele bekende ME experts, waaronder Dr. Weir, Dr. VanNess, Dr. van Elzakker, Dr. Zeineh, prof. Racaniello, Prof. Coyne, A. Whittemore, tekenden de petitie. Er zijn al bijna 3000 handtekeningen opgehaald. Iedere handtekening is nog steeds zeer welkom. Immers ME is geen SOLK, het biopsychosociaal model is niet van toepassing, CGT is geen behandeling. Een paradigmashift in het denken over ME is hard nodig!
Vandaag, op Wereld ME Dag 2016, het derde en laatste deel in deze serie. Daarin geven wij aandacht aan het feit dat patiënten zelf de afgelopen jaren een ongelooflijk belangrijke bijdrage hebben geleverd aan de wetenschap, door artikelen te schrijven in wetenschappelijke tijdschriften en/of kritische commentaren gepubliceerd te krijgen, en zo bijvoorbeeld de vele methodologische fouten van bijvoorbeeld CGT/GET-studies aan de kaak hebben gesteld. David Tuller en James Coyne prijzen de zeer belangrijke bijdragen die deze “citizen scientists” leveren aan het op gang krijgen van verandering voor ME. Voor dit derde deel van What about ME? zijn wij verheugd dat onze eigen citizen scientist van de lage landen, Frank Twisk, een gastblog getiteld “essentiële kwesties rond ME” schreef. Dank Frank voor al het werk al die jaren. En ga vooral door !
Essentiële kwesties m.b.t. ME
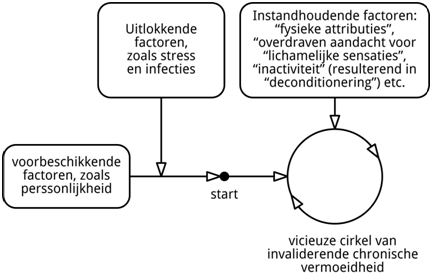
Ooit, zei de oude man, kon een ziek ME-de-mens zich verlaten op de expertise en het doorzettingsvermogen van de wetenschappers, de empathie en medische zorg van artsen en medisch-specialisten en de financiële en praktische ondersteuning door overheidsinstanties. Maar die tijd ligt inmiddels ver achter ons. Sinds de intrede van het marktdenken wordt de zieke geacht te bewijzen dat-ie echt ziek is en dat-ie wil genezen. Want wie wil genezen, die kán genezen in de New Age-filosofie die in het (bio)psychosociale “verklaringsmodel” (1,2) gestalte voor “CVS” heeft gekregen. De ME-de-patiënt wordt geacht zijn/haar ”herstelbelemmerende preoccupaties” (3) los te laten en zijn/haar gedrag aan te passen. Wie niet wil genezen van zijn/haar “bewegingsangst” (4), moet daarvoor zelf de medische en financiële consequenties dragen.
Omdat ME-de-patiënten vaak te maken hebben met die “omgekeerde bewijslast”, wil ik in deze bijdrage drie essentiële kwesties aan de orde stellen. Spijtig genoeg zijn ME-de-patiënten gedwongen “proactief” te zijn en een standpunt in te nemen. Als zieke kun je niet eenvoudig achterover leunen “om je ziektewinst te incasseren”…
De diagnose – ME, CVS en SEID: wat maakt het?
Volgens vermoeidheidsdeskundigen zijn Myalgische Encefalomyelitis (ME) en het chronisch vermoeidheidssyndroom (CVS) synoniemen (5), terwijl anderen, zoals prof. Jason (6) en prof. Maes (7), ME als “een ernstige variant van CVS” classificeren. Beide standpunten zijn feitelijk onjuist. Niet alle Noord-Hollanders (lees: CVS-patiënten) zijn Ajax-supporter (lees: ME-patiënt) en een aanzienlijk deel van de Ajax-aanhang (ME-patiënten) komt niet uit Noord-Holland (is geen CVS-patiënt). Om te begrijpen waarom een zuiver onderscheid essentieel is, is een korte geschiedenisles onontbeerlijk.
Myalgische Encefalomyelitis (ME)

Sinds de uitbraak in het LA County Hospital in Los Angeles 1934 (8) hebben over de hele wereld epidemieën van “atypische poliomyelitis” (9,10,11) plaatsgevonden. Eén van de meest bekende uitbraken is die in het Royal Free Hospital in Londen (12). In 1959 (13) werd ME als aparte diagnostische eenheid onderkend en sinds 1969 (14) is ME als neurologische ziekte door de Wereldgezondheidsorganisatie (WHO) geclassificeerd. Dr. Melvin Ramsay, die zich decennialang in de ziekte verdiepte, kwam op basis van eigen bevindingen en die van anderen uiteindelijk tot de volgende definitie:
|
De kenmerkende symptomen van ME (15,16,17,18,19):
Twee andere typische kenmerken van ME:
|
Dr. Melvin Ramsay |
Het begrip “vermoeidheid” speelt nauwelijks tot geen rol in de definities van Ramsay. De diagnose van ME mocht volgens Ramsay alleen gesteld worden als er sprake was van dagen aanhoudende spierzwakte en typerende neurologische verschijnselen.
Chronisch vermoeidheidssyndroom (CVS)
Veel van de huidige problemen zijn terug te voeren tot de introductie van het begrip CVS in 1988 (20). CVS werd o.l.v. Fukuda in 1994 (21) als volgt geherdefinieerd.
|
Dr Keiji Fukuda |
Het enige verplichte symptoom van CVS (21):
Daarnaast met minstens vier van de volgende symptomen:
|
Je hoeft geen wetenschappelijk wonderkind te zijn om in te zien dat iemand aan de diagnose ME kan voldoen zonder aan de eisen van CVS te voldoen, bijvoorbeeld omdat er geen sprake is van hoofdpijn, gewrichtspijn, zere keel, gevoelige lymfeklieren en spierpijn (in rust). Iemand kan de diagnose CVS krijgen zonder ook maar aan één kenmerk van ME te voldoen, bijvoorbeeld als iemand kampt met vermoeidheid, hoofdpijn, gewrichtspijn, zere keel, en niet-verkwikkende slaap (22).
Omdat de meeste studies sinds 1994 onderzoek betreft van mensen met CVS/chronische vermoeidheid (waarvan een deel aan de diagnose ME voldoet), hebben veel van die studies logischerwijs geen eensluidende conclusies opgeleverd. Een onderzoek naar de verzameling mensen die in Noord-Holland woont en/of Ajax-supporters is, kan en zal nooit één harde conclusie opleveren. Of zoals Desmond MacHale stelt:
|
|
De gemiddelde mens heeft één borst en één testikel. Emeritus Hoogleraar Wiskunde aan de University College Cork, Ierland |
Myalgische Encefalomyelitis (ME) volgens de Internationale Consensus-Criteria (ICC)
Teneinde de Babylonische spraakverwarring m.b.t. “ME/CVS’’ te reduceren, publiceerde een groep internationale wetenschappers in 2003 de Canadese consensus-criteria (CCC) voor ME/CVS (23). In vervolg daarop werden in 2011 de Internationale Consensus Criteria (ICC) voor ME (24) gepubliceerd. Naast nieuwe diagnosecriteria werd voorgesteld voortaan de naam ME te gebruiken en de naam CVS definitief te schrappen. Alhoewel de invoering van de ICC een stap voorwaarts zou betekenen t.o.v. CVS, moet worden geconstateerd dat de ICC op belangrijke punten afwijken van de oorspronkelijke definitie van ME (16,19), die “van onderuit” tot stand kwam. Ook, moet worden vastgesteld dat de ICC nog niet m.b.v. empirisch onderzoek gevalideerd zijn.
Persoonsafhankelijke definities van ME/CVS
In de tussentijd publiceerde de Centers of Disease Control (CDC) een nog ruimere definitie van CVS (25) en propageren verschillende wetenschappers hun eigen definities van “ME/CVS”, zoals de vier-symptomendefinitie van prof. Jason (26) en de Neuro-Inflammatoire en Oxidatieve Stress- Vermoeidheids (NIOF)-definitie van prof. Maes (27). Die persoonlijke definities dragen niet alleen bij tot meer verwarring, ze zijn ook geen goed alternatief. De vier-symptomendefinitie (26) is gebaseerd op het (onjuiste) uitgangspunt dat “ME/CVS” één ziekte is (ME is “een ernstige variant van CVS”). Op basis van de aanname werden vervolgens de meest voorkomende symptomen bepaald. Maar de meest voorkomende symptomen van wat? Van een niet-bestaande mengelmoes-verzameling. De NIOD-definitie (27), hoe goed bedoeld ook, brengt een heel ander probleem met zich mee. In plaats van de diagnosecriteria aangescherpt worden (bijvoorbeeld tot ME), wordt de definitie verruimd tot een grote verzameling “inflammatoire aandoeningen”. Als een probleem (ME en CVS) ingewikkeld is, moet je die twee problemen ontrafelen en niet het probleem nog groter maken dan het al is.
Systemic Exertion Intolerance Disease (SEID)
In 2015 introduceerde het Institute of Medicine (IOM) met veel bombarie een nieuwe naam voor “ME/CVS”, systemische inspanningsintolerantieziekte (SEID), en nieuwe diagnosecriteria (28). Veel patiënten omarmden vrijwel direct de voorstellen van het IOM, omdat het rapport eindelijk recht deed aan de ernst van “de” ziekte ME/CVS.
|
|
Verplichte symptomen voor de diagnose SEID (28):
én één of twee van de volgende twee symptomen:
|
Het IOM stelt ten onrechte dat ME en CVS vergelijkbare ziektebeelden zijn (28). SEID is gebaseerd op basis van studies die voor het overgrote deel betrekking hebben op CVS-onderzoek. Oudere studies, m.n. ME-studies, zijn niet in de analyse betrokken. Het is dus niet verwonderlijk dat SEID, dat, volgens het IOM, ME (15,16,17,18,19) en CVS (21) zou moeten vervangen, het best aangeduid kan worden als CVS 2.0. SEID doet op geen enkele wijze recht aan de (originele) definitie van ME (29,30). Sterker, niet één van de kenmerkende symptomen (zie boven) is verplicht voor de diagnose SEID. De diagnosecriteria van SEID zijn niet veel stringenter dan de criteria voor CVS (21), terwijl aan de andere kant, mede omdat begrippen zoals vermoeidheid en postexertionele “malaise” subjectief zijn en niet geobjectiveerd hoeven te worden (28), grote groepen patiënten met andere medische en psychische aandoeningen aan de diagnosecriteria voor SEID voldoen (30). Met de introductie van SEID wordt de wetenschappelijke verwarring, die ontstaan is met de introductie van CVS, compleet.
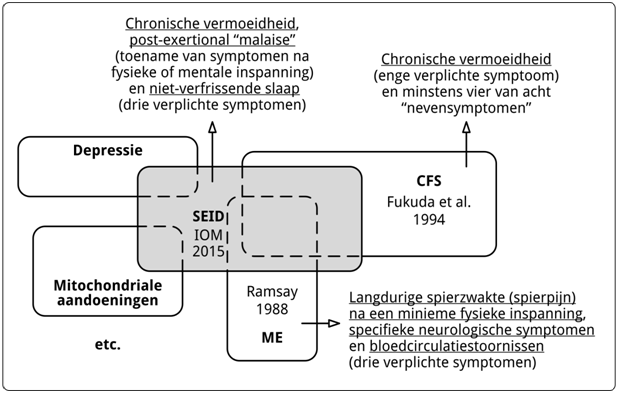
De conclusies op basis van de definities van ME (15,16,17,18,19), CVS (21) en SEID (28) zijn glashelder: ME is géén CVS, en SEID is geen goed alternatief voor CVS, laat staan ME. Dat heeft niets met mijn voorkeuren te maken, zoals onterecht in het IOM-rapport gesteld wordt (28), bladzijde 31, maar met de diagnosecriteria (definities).
De discussie over de naam staat los van de discussie m.b.t. de diagnosecriteria!
De ziekte: zijn de symptomen “hard te maken”?
Een tweede misverstand ontstaat als mensen, bewust of onbewust, onverklaard als synoniem opvatten van aan onecht (psychogeen: door de geest veroorzaakt). Dat symptomen nog niet (helemaal) verklaard kunnen worden, betekent niet dat ze geen fysieke oorzaak hebben. Als de computer het aantoonbaar niet doet en de oorzaak nog niet achterhaald is, gaat men het probleem toch ook niet ontkennen. Het is dus, zowel voor de individuele patiënt (om de “ongelovigen” met harde feiten te kunnen confronteren) als voor wetenschappers (teneinde effectief onderzoek uit te voeren), essentieel dat kenmerkende symptomen geobjectiveerd (“hard gemaakt”) worden.
De twee essentiële problemen in de diagnose van ME (15,16,17,18,19), CVS (21) en SEID (28) hebben betrekking op de diagnosecriteria (zie vorige paragraaf) en de wijze waarop de symptomen vastgesteld worden: aan de hand van vragenlijstjes, zoals de veel gebruikte DePaul Questionnaire, óf op basis van uitslagen van objectieve testen, zoals neurocognitieve testen, (herhaalde) inspanningstesten en kanteltafeltesten.
Het probleem met een “subjectieve diagnose” is tweeledig. Subjectieve begrippen zoals “vermoeidheid”, “postexertionele malaise” en “niet-verkwikkende slaap” zijn persoonsafhankelijk: wat is mijn vermoeidheidsscore van 80 waard vergeleken met die van een andere patiënt? en ongrijpbaar: wat stelt een (gevoelsmatige) verbetering van 80 naar 70 door gedragstherapie (CGT), progressieve inspanningstherapie (GET), Ampligen of Rituximab voor als die niet gepaard gaat met een objectieve verbetering, zoals een betere zuurstofopname of een hoger activiteitenniveau (31)? Niet alleen zijn begrippen zoals “vermoeidheid” en “inspanningsintolerantie” subjectief en ongrijpbaar, ook zullen mensen met andere ziekten en aandoeningen aan de diagnosecriteria voldoen, zoals mensen met burn-out en mitochondriale ziekten. Omdat het IOM, in weerwil van ”mijn” aanbeveling zoals vermeld in het rapport (28) bladzijde 264, objectieve testen min of meer naar de prullenbak verwijst, voldoen patiënten met “chronische vermoeidheid”, mensen met andere medische aandoeningen en mensen met psychische problemen ook aan de diagnosecriteria voor SEID (32).
Karakteristieke symptomen, met name postexertionele “malaise”, zouden m.i. zo veel mogelijk m.b.v. bestaande, alom geaccepteerde en vaak relatief goedkope testen, geobjectiveerd (in harde getallen uitgedrukt) moeten worden: zie tabel 1 (33).
Met bestaande, relatief goedkope testen kunnen tevens de diverse aspecten van postexertionele malaise (fysiek, mentaal, spierzwakte) geobjectiveerd worden (34)
|
“Meten is weten” Nou je het zegt: die dokter lijkt wel op mijn leraar wiskunde |
|
Natuurlijk besef ik me terdege dat sommige testen enorm belastend zijn voor patiënten en dat “ernstige gevallen” de testen niet kúnnen ondergaan. Voor de patiënt die, met alle gevolgen van dien, de testen wel zou kunnen ondergaan, is het een “keuze tussen twee kwaden”! Maar gezien het onbegrip en de serieuze problemen waarin je als patiënt terecht kan komen, is het goed te weten dat er wel een alternatief is (33).
|
Symptoom |
Testen |
|
|
Fysieke zwakheid: ”vermoeidheid”, ”gebrek aan energie” |
Cardiopulmonale inspanningstesten (CPET): maximale werklast (inspanningsvermogen) en zuurstofopname bij uitputting (VO2max) en zuurstofopname en werklast bij de anaerobe drempel (“verzuringsdrempel”) |
|
|
Cognitieve symptomen: concentratieproblemen etc. |
Specifieke neuropsychologische testen |
|
|
Post-exertionele “malaise” |
||
|
|
Fysieke effecten |
Herhaalde cardiopulmonale inspanningstesten, met 24 uur tussenpauze |
|
|
Cognitieve effecten |
|
|
||
|
Spierzwakte |
Spieronderzoek m.b.v. dynamometers (eventueel herhaald na 24 uur): spierkracht, uithoudingsvermogen en “herstel” |
|
|
Orthostatische intolerantie |
Kanteltafeltest |
|
|
Verminderde stressbestendigheid |
Hormonaal onderzoek (HPA-as en schildklier)
|
|
|
Slaapstoornissen |
|
|
|
Visuele symptomen |
|
|
|
||
Voor referenties zie de Engelstalige versie van deze overzichtstabel (33): klik hier.
De behandeling: zijn CGT en GET evidence based effectief?
Regelmatig wordt door pleitbezorgers van het (bio)psychosociale “verklaringsmodel” beweerd dat CGT en GET bewezen (“evidence-based”) effectieve behandelingen zijn.
Een uitgebreide analyse van gerandomiseerd onderzoek met controlegroep-studies (RCTs) (circa 90 studies, uitkomsten nog niet gepubliceerd), leert het volgende:
- grofweg de helft van de studies, zoals de studie van Prins (2) die de basis vormde voor het advies van de Gezondheidsraad in 2005 (5), en de fel bekritiseerde PACE trial-studie (35), heeft betrekking op mensen met chronisch vermoeidheid, niet op patiënten met de diagnose CVS (21), laat staan om ME-patiënten (16,19);
- de criteria voor verbetering zijn veelal subjectieve maatstaven, zoals “vermoeidheid” (Chalder vermoeidheidsscore/CFB (36), CIS vermoeidheid (37)), “fysiek functioneren” (SF-36 (38,39,40)) en “beperkingen” (Sickness Impact Profile-8 (41,42));
- in circa de helft van de studies wordt een (kleine) subjectieve verbetering vastgesteld (vaak in een kleine deelgroep van mensen met chronische vermoeidheid);
- de criteria voor subjectieve maatstaven voor “herstel” en “verbetering” verschillen vaak per studie en soms zelfs binnen één studie, zo dat mensen met een CIS F-score (37) < 35 en een SIP8-score (41,42) < 700 volgens een studie hersteld zijn van CVS, terwijl tegelijkertijd onderkend wordt dat een CIS F-score (37) < 27 en een SIP8-score (41,42) < 203 “normale waarden” zijn (43), en dat mensen die voor de studie als “ernstig vermoeid” (CFB ≥ 6) en “ernstig beperkt” (SF-36 PF ≤ 65) gekwalificeerd worden (44) na afloop met dezelfde of slechtere scores genezen verklaard worden (CFL ≤ 18, overeenkomend met CFB ≤ 9), en SF-36 PF ≥ 60) (45).
- als we kijken naar objectieve graadmeters die in CGT/GET-studies gebruikt zijn:
- is er in een paar studies sprake van een (kleine) verbetering, bijvoorbeeld van de zuurstofopname, maar dan is de verbetering minimaal (46) of is er gezien de “prestaties vooraf” hoogstwaarschijnlijk geen sprake van CVS (47),
- is er meestal geen verbetering, bijvoorbeeld van het activiteitenniveau (48), en
- is er in een aantal studies zelfs sprake van een verslechtering, bijvoorbeeld een afname van de maximale zuurstofopname (49) of arbeidsparticipatie (50).
In het kort samengevat: CGT en GET hebben een (relatief klein) positief effect op een kleine groep patiënten met chronische vermoeidheid en dat dan alleen nog maar in subjectieve termen, zoals “vermoeidheid” en “fysiek functioneren”. Objectief gezien is er geen enkel bewijs dat CGT en GET tot verbetering, laat staan herstel, leidt in CVS (21). Onderzoek naar het effect van CGT en GET in ME (16,19) is nimmer uitgevoerd. Deze conclusies worden bevestigd door de uitkomsten van de omstreden PACE trial.
De PACE-studie uit 2011 (35) liet zien dat CGT en GET een (klein) positief effect heeft op een kleine groep mensen met chronische vermoeidheid (CGT: 30% van de deelnemers, GET: 28%, standaardzorg: 14%, placebo-effect psychologische interventies: 14% (51)). Een opvolgstudie (52) liet zien dat er ±2 jaar geen verschil is tussen pacing en van standaardzorg en CGT en GET, zelfs bij mensen met chronisch vermoeidheid.
Alhoewel het aantal meters die in 6 minuten gelopen werd, iets verbeterde, was de prestatie na afloop volstrekt onvoldoende om te kunnen spreken van herstel (53).
In weerwil van het door de onderzoekers gesuggereerde herstel van 22% van de patiënten m.b.v. CGT en GET, was er geen enkele verbetering in objectieve termen:
re-integratie (54), gebruik van medische en sociale voorzieningen (54) of fitheid (55).

“CBT and GET can safely be added to SMC to moderately improve outcomes for chronic fatigue syndrome, but APT[pacing] is not an effective addition.” (35).
“This study confirms that recovery from CFS is possible, and that CBT and GET are the therapies most likely to lead to recovery.” (45)
Als we kijken naar (soms grootschalig) onderzoek onder patiënten (56,57) en een onderzoek uit België (50), dan kunnen we zelfs stellen dat CGT en GET meestal niet effectief zijn en dat een grote groep patiënten verslechtert na CGT maar vooral na GET.
Een gedegen analyse van de PACE-trial data lijkt die conclusie te onderstrepen (58).
Conclusie
Wellicht tot vervelens toe, waarvoor bij voorbaat mijn verontschuldigingen, snijdt deze column drie centrale kwesties aan die essentieel zijn voor het behartigen van het eigen belangen en het belang van ME-de-patiënten. Die centrale “issues” zijn:
- ME is géén CVS en “ME/CVS” kan dus ook niet door SEID vervangen worden;
- Symptomen moeten in het individuele belang (belang van de patiënt) en het algemeen belang (de wetenschap) zo veel mogelijk geobjectiveerd worden;
- CGT en GET zijn geen evidence-based effectieve behandelingen en er zijn zelfs aanwijzingen dat CGT en GET schadelijk zijn voor grote groepen patiënten.
Als ME-de-patiënten en zelfverklaarde vertegenwoordigers daadwerkelijk vooruitgang willen boeken, zullen ze zich hard moeten maken voor (verificatie en gebruik) van de oorspronkelijke ME-criteria (16,19), SEID als “niet ter zake doende” terzijde moeten schuiven, aan moeten dringen op objectieve testmethoden en de “evidence-based” effectiviteitsclaim met de beschikbare feiten en argumenten moeten ontkrachten.
- Vercoulen JH, Swanink CM, Galama JM, Fennis JF, Jongen PJ, Hommes OR, et al. The persistence of fatigue in chronic fatigue syndrome and multiple sclerosis: development of a model. J Psychosom Res. 1998; 45(6):507-517. PMID: 9859853. doi: 10.1016/S0022-3999(98)00023-3.
- Prins JB, Bleijenberg G, Bazelmans E, Elving LD, de Boo TM, Severens JL, et al. Cognitive behaviour therapy for chronic fatigue syndrome: a multicentre randomised controlled trial. Lancet. 2001; 357(9259):841-847. PMID: 11265953. doi: 10.1016/S0140-6736(00)04198-2.
- Knoop H, Bleijenberg G. Belemmerende preoccupaties bij patiënten met het chronisch vermoeidheidssyndroom. Directieve Therapie. 2005; 25(5):105-111. doi: 10.1007/BF03060384.
- Twisk FNM. Post-exertional malaise in chronic fatigue syndrome. Lancet Psychiatry. 2015; 2(4):e8–e9. doi: 10.1016/S2215-0366(15)00044-9.
- Gezondheidsraad. Het chronische-vermoeidheidssyndroom. Publicatie nr. 2005/02. https://www.gezondheidsraad.nl/sites/default/files/0502nrv.pdf. Den Haag: Gezondheidsraad; 2005. ISBN 90-5549-554-9.
- Jason LA, Kot B, Sunnquist M, Brown A, Evans M, Jantke R, et al. Chronic fatigue syndrome and myalgic encephalomyelitis: towards an empirical case definition. Health Psychol Behav Med. 2015; 3(1):82-93. doi: 10.1080/21642850.2015.1014489.
- Maes M, Anderson G, Morris G, Berk M. Diagnosis of myalgic encephalomyelitis: where are we now? Expert Opin Med Diagn. 2013; 7(3):221-225. PMID: 23480562. doi: 10.1517/17530059.2013.776039.
- Gilliam AG. Epidemiological study on an epidemic, diagnosed as poliomyelitis, occurring among the personnel of Los Angeles County General Hospital during the summer of 1934. United States Treasury Department Public Health Service Public. Health Bulletin 240. 1938:1–90.
- Parish JG. Early outbreaks of ‘epidemic neuromyasthenia’. Postgrad Med J. 1978; 54(637):711-717. PMID: 370810. doi: 10.1136/pgmj.54.637.711.
- Sigurdsson B, Sigurjonsson J, Sigurdsson JH, Thorkelsson J, Gudmundsson KR. A disease epidemic in Iceland simulating poliomyelitis. Am J Hyg. 1950; 52(2):222-238. PMID: 14771044.
- Wallis AL. An investigation into an unusual disease seen in epidemic and sporadic form in a general practice in Cumberland in 1955 and subsequent years. MD Thesis. Edinburgh: University of Edinburgh; 1957. https://www.era.lib.ed.ac.uk/bitstream/handle/1842/9382/ Wallis1957_FULL.pdf.
- Crowley N, Nelson M, Stovin S. Epidemiological aspects of an outbreak of encephalomyelitis at the Royal Free Hospital, London, in the summer of 1955. J Hyg (Lond). 1957; 55(1):102-122. PMID: 13416578. doi: 10.1017/S0022172400061295.
- Acheson ED. The clinical syndrome variously called benign myalgic encephalomyelitis, Iceland disease and epidemic neuromyasthenia. Am J Med. 1959; 26(4):569-595. PMID: 13637100. doi: 10.1016/0002-9343(59)90280-3.
- WHO. International Classification of Diseases, Eighth Revision (ICD-8). 1967; I: 158 (code 323).
- Ramsay AM. Encephalomyelitis in North West London; an endemic infection simulating poliomyelitis and hysteria. Lancet. 1957; 273(7007):1196-1200. PMID: 13492606. doi: 10.1016/S0140-6736(57)90163-0.
- Ramsay AM. Myalgic encephalomyelitis and postviral fatigue states: the saga of Royal Free disease. 2nd ed. London, UK: Gower Publishing Corporation; 1988.
- Ramsay AM. The clinical identity of the Myalgic Encephalomyelitis syndrome. ME Association. 1988. http://web.onetel.com/~kickback/THE%20CLINICAL%20IDENTITY%20OF%20ME.html.
- Ramsay AM. Myalgic encephalomyelitis, or what? Lancet. 1988; 332(8602):100. PMID: 2898668. doi: 10.1016/S0140-6736(88)90028-1.
- Ramsay AM, Dowsett EG. Myalgic Encephalomyelitis: Then and now. In Hyde BM, Goldstein J, Levine P, editors. The Clinical and Scientific Basis of Myalgic Encephalomyelitis / Chronic Fatigue Syndrome. Ottawa: The Nightingale Research Foundation; 1992.
- Holmes GP, Kaplan JE, Gantz NM, Komaroff AL, Schonberger LB, Straus SE, et al. Chronic fatigue syndrome: a working case definition. Ann Intern Med. 1988; 108(3):387-389. PMID: 2829679. doi: 10.7326/0003-4819-108-3-387.
- Fukuda K, Straus SE, Hickie I, Sharpe M, Dobbins JG, Komaroff AL. The chronic fatigue syndrome: a comprehensive approach to its definition and study. Ann Intern Med. 1994; 121(12):953-959. PMID: 7978722. doi: 10.7326/0003-4819-121-12-199412150-00009.
- Jason LA, Katz BZ, Mears C, Jantke R, Abby A, Sunnquist M, et al. Issues in estimating rates of pediatric chronic fatigue syndrome and Myalgic Encephalomyelitis in a community-based sample. J Neuro Psych Physio. 2015 Dec; 21:e37281 (in press). doi: 10.17795/ajnpp-37281.
- Carruthers BM, Jain AK, de Meirleir K, Peterson DL, Klimas NG, Lerner AM, et al. Myalgic encephalomyelitis/chronic fatigue syndrome: clinical working case definition, diagnostic and treatment protocols. Journal of Chronic Fatigue Syndrome. 2003; 11(1):7-115. doi: 10.1300/J092v11n01_02.
- Carruthers BM, van de Sande MI, de Meirleir KL, Klimas NG, Broderick G, Mitchell T, et al. Myalgic encephalomyelitis: international consensus criteria. J Intern Med. 2011; 270(4):327-338. PMID: 21777306. doi: 10.1111/j.1365-2796.2011.02428.x.
- Reeves WC, Wagner D, Nisenbaum R, Jones JF, Gurbaxani B, Solomon L, et al. Chronic fatigue syndrome: a clinically empirical approach to its definition and study. BMC Medicine. 2005; 3:19. PMID: 16356178. doi: 10.1186/1741-7015-3-19.
- Jason LA, Sunnquist M, Brown A, Furst J, Cid M, Farietta J, et al. Factor analysis of the DePaul symptom questionnaire: identifying core domains. J Neurol Neurobiol. 2015; 1(4). PMID: 27088131. doi: 10.16966/2379-7150.114.
- Maes M. A new case definition of Neuro-Inflammatory and Oxidative Fatigue (NIOF), a neuroprogressive disorder, formerly known as chronic fatigue syndrome or Myalgic Encephalomyelitis: results of multivariate pattern recognition methods and external validation. Neuro Endocrinol Lett. 2015; 36(4):320-329. PMID: 26454487.
- IOM (Institute of Medicine). Beyond myalgic encephalomyelitis/chronic fatigue syndrome: redefining an illness. Washington, DC: 2015. ISBN: 978-0-309-31689-7.
- Twisk FNM. A critical analysis of the proposal of the Institute of Medicine to replace Myalgic Encephalomyelitis and Chronic Fatigue Syndrome by a new diagnostic entity called Systemic Exertion Intolerance Disease. Curr Med Res Opin. 2015; 31(7):1333-1347. PMID: 25912615. doi: 10.1185/03007995.2015.1045472.
- Twisk FNM. Replacing Myalgic Encephalomyelitis and chronic fatigue syndrome with Systemic Exercise Intolerance Disease is not the way forward. Diagnostics (Basel). 2016; 6(1): 10. PMID: 26861399. doi: 10.3390/diagnostics6010010.
- Twisk FNM. A definition of recovery in myalgic encephalomyelitis and chronic fatigue syndrome should be based upon objective measures. Qual Life Res. 2014; 23(9):2417-2418. PMID: 24935018. doi: 10.1007/s11136-014-0737-1.
- Jason LA, Sunnquist M, Kot B, Brown A, Reed J. Unintended consequences of not specifying exclusionary illnesses with systemic exertion intolerance disease. Diagnostics. 2015; 5(2):272-286. doi:10.3390/diagnostics5020272.
- Twisk FNM. Accurate diagnosis of Myalgic Encephalomyelitis and chronic fatigue syndrome based upon objective test methods for characteristic symptoms. World J Methodol. 2015; 5(2):68-87. doi: 10.5662/wjm.v5.i2.68.
- Twisk FNM. Objective evidence of post-exertional “malaise” in Myalgic Encephalomyelitis and chronic fatigue syndrome. J Sports Med Doping Stud. 2015; 5(2):159. doi: 10.4172/2161-0673.1000159.
- White PD, Goldsmith KA, Johnson AL, Potts L, Walwyn R, DeCesare JC, et al. Comparison of adaptive pacing therapy, cognitive behaviour therapy, graded exercise therapy, and specialist medical care for chronic fatigue syndrome (PACE): a randomised trial. Lancet. 2011; 377(9768):823-836. PMID: 21334061. doi: 10.1016/S0140-6736(11)60096-2.
- Chalder T, Berelowitz G, Pawlikowska T, Watts L, Wessely S, Wright D, et al. Development of a fatigue scale. J Psychosom Res. 1993; 37(2):147-153. PMID: 8463991. doi: 10.1016/0022-3999(93)90081-P.
- Vercoulen JHMM, Alberts M, G B. De Checklist Individual Strength (CIS). Gedragstherapie. 1999; 32(2):131-136.
- Ware JEJ, Sherbourne CD. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection. Med Care. 1992; 30(6):473-483. PMID: 1593914. doi: 10.1097/00005650-199206000-00002.
- McHorney CA, Ware JEJ, Raczek AE. The MOS 36-Item Short-Form Health Survey (SF-36): II. Psychometric and clinical tests of validity in measuring physical and mental health constructs. Med Care. 1993; 31(3):247-263.PMID: 8450681. doi: 10.1097/00005650-199303000-00006.
- McHorney CA, Ware JEJ, Lu JF, Sherbourne CD. The MOS 36-item Short-Form Health Survey (SF-36): III. Tests of data quality, scaling assumptions, and reliability across diverse patient groups. Med Care. 1994; 32(1):40-66. PMID: 8277801. doi: 10.1097/00005650-199401000-00004.
- Vercoulen JH, Swanink CMA, Fennis JFM, Galama JMD, van der Meer JWM, Bleijenberg G. Dimensional assessment of chronic fatigue syndrome. J Psychosom Res. 1994; 38(5):383-392. PMID: 7965927. doi: 10.1016/0022-3999(94)90099-X.
- Bergner M, Bobbitt RA, Carter WB, Gilson BS. The Sickness Impact Profile: development and final revision of a health status measure. Med Care. 1981; 19(8):787-805. PMID: 7278416. doi: 10.1097/00005650-198108000-00001.
- Knoop H, Bleijenberg G, Gielissen MF, van der Meer JWM, White PD. Is a full recovery possible after cognitive behavioural therapy for chronic fatigue syndrome? Psychother Psychosom. 2007; 76(3):171-176. PMID: 17426416. doi: 10.1159/000099844.
- White PD, Sharpe MC, Chalder T, DeCesare JC, Walwyn R, group Pt. Protocol for the PACE trial: a randomised controlled trial of adaptive pacing, cognitive behaviour therapy, and graded exercise, as supplements to standardised specialist medical care versus standardised specialist medical care alone for patients with the. BMC Neurol. 2007; 7:6. PMID: 17397525. doi: 10.1186/1471-2377-7-6.
- White PD, Goldsmith KA, Johnson AL, Chalder T, Sharpe M, Group. PTM. Recovery from chronic fatigue syndrome after treatments given in the PACE trial. Psychol Med. 2013; 43(10):2227-2235. PMID: 23363640. doi: 10.1017/S0033291713000020.
- Wallman KE, Morton AR, Goodman C, Grove R, Guilfoyle AM. Randomised controlled trial of graded exercise in chronic fatigue syndrome. Med J Aust. 2004; 180(9):444-448. PMID: 15115421.
- Fulcher KY, White PD. Randomised controlled trial of graded exercise in patients with the chronic fatigue syndrome. BMJ. 1997; 314(7095):1647-1652. PMID: 9180065. doi: 10.1136/bmj.314.7095.1647.
- Wiborg JF, Knoop H, Stulemeijer M, Prins JB, Bleijenberg G. How does cognitive behaviour therapy reduce fatigue in patients with chronic fatigue syndrome? The role of physical activity. Psychol Med. 2010; 40(8):1281-1287. PMID: 20047707. doi: 10.1017/S0033291709992212.
- Moss-Morris R, Sharon C, Tobin R, Baldi JC. A randomized controlled graded exercise trial for chronic fatigue syndrome: outcomes and mechanisms of change. J Health Psychol. 2005; 10(2):245-259. PMID: 15723894. doi: 10.1177/1359105305049774.
- Akkoordraad in het kader van de revalidatieovereenkomsten inzake ten laste neming door Referentiecentra van patiënten lijdend aan het Chronisch vermoeidheidssyndroom. Evaluatierapport (2002-2004) m.b.t. de uitvoering van de revalidatieovereenkomsten tussen het Comité van de verzekering voor geneeskundige verzorging (ingesteld bij het RIZIV) en de Referentiecentra voor het Chronisch vermoeidheidssyndroom. juli 2006.
- Cho HJ, Hotopf M, Wessely S. The placebo response in the treatment of chronic fatigue syndrome: a systematic review and meta-analysis. Psychosom Med. 2005; 67(2):301-313. PMID: 15784798. doi: 10.1097/01.psy.0000156969.76986.e0.
- Sharpe M, Goldsmith KA, Johnson AL, Chalder T, Walker K, White PD. Rehabilitative treatments for chronic fatigue syndrome: long-term follow-up from the PACE trial. Lancet Psychiatry. 2015; 2(12):1067-1074. PMID: 26521770. doi: 10.1016/S2215-0366(15)00317-X.
- Twisk FNM. PACE: CBT and GET are not rehabilitative therapies. Lancet Psychiatry. 2016; pii: S2215-0366(15)00554-4. PMID: 26795758. doi: 10.1016/S2215-0366(15)00554-4.
- McCrone P, Sharpe M, Chalder T, Knapp M, Johnson AL, Goldsmith KA, et al. Adaptive pacing, cognitive behaviour therapy, graded exercise, and specialist medical care for chronic fatigue syndrome: a cost-effectiveness analysis. PLoS One. 2012; 7(8):e40808. PMID: 22870204. doi: 10.1371/journal.pone.0040808.
- Chalder T, Goldsmith KA, White PD, Sharpe M, Pickles AR. Rehabilitative therapies for chronic fatigue syndrome: a secondary mediation analysis of the PACE trial. Lancet Psychiatry. 2015; 2(2):141-152. PMID: 26359750. doi: 10.1016/S2215-0366(14)00069-8.
- ME Association. “No decisions about me without me”. ME/CFS illness management survey results, part 1. Gawcott, Bucks (England): 2015. http://www.meassociation.org.uk/wp-content/uploads/2015-ME-Association-Illness-Management-Report-No-decisions-about-me-without-me-30.05.15.pdf.
- Twisk FNM, Arnoldus RJW, Maes M. ME/CVS, de psychotherapeut en de (on)macht van het evidence-beest. Tijdschr Psychother. 2011; 37(4):233-258. doi: 10.1007/s12485-011-0042-1.
- Vink, M. The PACE trial invalidates the use of cognitive behavioral and graded exercise therapy in Myalgic Encephalomyelitis/chronic fatigue syndrome: A review. J Neurol Neurobiol. 2016; 2(3): doi: 10.16966/2379-7150.124.
© Frank Twisk voor ME-gids
Lees ook
- What About ME? Deel II: ME-patiënten starten petitie “ME is geen SOLK” n.a.v. bekendmaking Gezondheidsraad (Update 3)
- What About ME? Deel 1: ME-patiënten vragen patiëntenorganisaties kleur te bekennen t.a.v. PACE