
Jaime S., #MEAction, 30 augustus 2016
Robert Naviaux, onderzoeker aan de Universiteit van Californië in San Diego, publiceerde onlangs een mijlpaalstudie over de metabolieten in patiënten met ME/cvs. Ze haalde wereldwijd het nieuws [behalve in België en Nederland…, n.v.d.r.]. Hieronder een diepteanalyse van de bevindingen van de paper en de gevolgen ervan.
Opmerking: een deel van onderstaande info is speculatief, en linkt Naviauxs bevindingen aan ander onderzoek. Bevindingen die niet expliciet door de studie aangegeven zijn, staan op het einde van het artikel samengevat.
Inleiding
Voor hen die zich afvragen wat de resultaten en de gevolgen zijn: kort gezegd stelt Naviauxs studie dat de cellen van ME-patiënten in een soort beschermende hibernatie [soort winterslaap, n.v.d.r.] zitten, waarbij ze hun consumptie van hulpbronnen beperken en zich in een hypometabolische staat zetten als antwoord op een infectie of andere stressor. Door de metabolieten van patiënten in detail te bestuderen, ontdekte men dat deze graad van beschermende hibernatie direct gecorreleerd is met de klinische graad van ernst.
Naviaux werpt ook op dat cellen bij ME/cvs cellen zijn onder enorme stress, waardoor ze een reeks verdedigingsmechanismes creëren, alsof ze een groot slot en alarmsysteem installeren en al hun waardevolle spullen verstoppen. Maarsommige pathogenen (ziekteverwekkers, n.v.d.r.) kennen de code om binnen te raken, en als de hulpbronnen verstopt zijn, kan de gastheer er ook niet aan. Beide aspecten van deze cellulaire verdedigingsmodus hebben diepgaande gevolgen op vlak van symptomatologie.
Naviauxs studie lichtte verschillen uit tussen mannelijke en vrouwelijke patiënten die nog nooit in andere studies beschreven werden:
- Vrouwen, maar niet mannen, hadden over het algemeen een verstoord vetzuur- en endocannabinoïde-metabolisme.
- Mannen, maar niet vrouwen, vertoonden algemeen gezien verhoogde concentraties aan (de aminozuren, n.v.d.r.) serine en threonine.
Maar de meerderheid van de bevindingen toonde afwijkende waarden aan bij beide geslachten, zoals verminderde cholesterolsynthese in één reactiepad en verminderde sfingolipiden en glycosfingolipiden.
Glycosfingolipiden, sfingolipiden en cholesterolsynthese zijn laag – en dat is een enorm belangrijk punt
Depletie van sfingolipiden zou al heel wat van de afwijkingen die we zien bij ME/cvs, kunnen verklaren.Ceramiden, een product van sfingolipiden, zijn verantwoordelijk voor het creëren van zogenaamde ‘ lipidevlotten‘, die zich tijdens infectie mobiliseren en aggregeren. Lipidevlotten hebben ook cholesterol en andere vetmoleculen nodig om goed te functioneren.
Ooit geloofde men dat membraaneiwitten en vetten altijd lukraak verspreid waren in de lipidendubbellaag waaruit het celmembraan bestaat.
Wat staat in elke biologiehandboek dat je ooit hebt gelezen.
© OpenStax via Wikimedia Commons (CC BY 4.0)
Maar nu is er een theorie dat er lipiderijke gebieden zijn in het membraan die vol zitten met glycosfingolipiden (suiker-amino-acohol-vetstukjes), cholesterol, gangliosiden en proteïnes. Ze vormen kleine ‘zakjes’, hoewel ze ook lineair kunnen zijn; en ze bundelen zich meestal op die manier als de cel gestresseerd is. Stress betekent in dit geval eender wat de cel mogelijk schade kan berokkenen, en suggereert niet dat deze cellen bang of overstuur zijn. (Voor zover wij weten zijn cellen niet zo emotioneel.)
De manier waarop zij samen functioneren in deze situaties, is complex en het zou kunnen dat hier een hoop proteïnes en vetten voor nodig zijn die een klein netwerk vormen, voortgetrokken door actine. Als één van deze proteïnes of vetten uiteenvallen, verliezen de membraanvlotten aan functionaliteit. En wat ze doen, is heel belangrijk: ze helpen de structurele integriteit van de cel behouden, en spelen tegelijkertijd ook een rol in de immuniteit. Caveolines en cavines, chemische stoffen die deel uitmaken van lipidevlotten, kunnen immuunactivering aanwakkeren of belemmeren, en spelen ook een rol in de neuronale signalering; en de verhouding caveoline tot cavine beïnvloedt vaak signalering van inflammatoire reactiepaden.
Om de cel te verdedigen, worden lipidevlotten geaggregeerd, waardoor het moeilijker wordt voor pathogenen om binnen te komen. Maar sommige bacteriële en virale pathogenen zijn geëvolueerd om deze verdediging niet alleen te omzeilen, maar ze ook uit te buiten. Door ‘binnen te glippen’ via de cellulaire achterdeur ontsnappen deze pathogenen ook aan de afvoer naar het lysosoom en mogelijk overleven ze daardoor langer dan hun traditioneel infectieuze tegenhangers.
Pathogenen die geëvolueerd zijn om de cel binnen te dringen via lipidevlotten
|
Bacteriën |
Virussen |
|
Pseudomonas aeruginosa [55] en [66] |
HIV-1 |
Het lijkt erop dat bepaalde schimmels dit mechanisme ook gebruiken, alhoewel schimmelpathogenen het minst bestudeerde van de drie pathogeentypes is als het gaat om hun interactie met lipidevlotten.
Downregulatie van de synthese van sfingolipiden in het algemeen, en van de synthese van ceramiden in het bijzonder, maken mogelijk deel uit van een gastheer-afweerreactie in aanwezigheid van deze pathogenen om te voorkomen dat ze binnendringen, om het risico te verminderen van cellulaire apoptose in reactie op infectie. Het zou ook kunnen dat de cellen de vorming van lipidevlotten upreguleren als een voortdurende beschermingsmaatregel, wat resulteert in de aanwezigheid van minder bij dit proces betrokken vrije lipiden.
De connectie tussen lipidevlotten en Rituximab
Fluge en Mella publiceerden kortgeleden een studie waarin stond dat B-celoverlevingsfactoren APRIL en BAFF waarschijnlijk niet de reden waren van het succes van Rituximab bij het verminderen van de symptomen van ME-patiënten. Als blijkt dat de studie van Naviaux et al. repliceerbaar is, zouden zijn bevindingen zowel kunnen verklaren waarom kanker meer voorkomt bij ME-patiënten, als waarom Rituximab voor sommigen werkt. Van George en Wu (2012),
Rituxan/Rituximab, een anti-CD20-antilichaam dat klinisch wordt ingezet om CD20-gemedieerde apoptose uit te lokken, werd gebruikt voor het bestuderen van het activeringsmechanisme van CD20. Na activering verplaatste CD20 zich naar het celterrein van de lipidevlotten, waar ze geactiveerd werden om apoptose in te leiden.
Met andere woorden: het zou kunnen dat Rituximab bij ME werkt doordat het in de lipidevlotten de nodige uiteenval veroorzaakt om pathogenen ervan te weerhouden via de ‘achterdeur’ de cel binnen te kruipen in het geval van een actieve infectie; of het zou kunnen dat het enkel cellen die zich in een afweertoestand bevinden dwingt tot vernietiging, met als gevolg een waterval aan metabolische gebeurtenissen die er uiteindelijk voor zorgen dat de meerderheid van de cellen zich niet langer in metabolische hibernatie bevindt. Dit zou deels de vertraagde werking van Rituximab kunnen verklaren, als het proces met zich meebrengt dat cellen in hibernatie langzaam maar zeker vervangen worden door gezondere exemplaren, en dat die cellen zich gaan vermeerderen. Het zou dan gaan om een geleidelijk proces, en geen ogenblikkelijke gebeurtenis.
Het doen uiteenvallen van lipiden is ook wat Rituximab doeltreffend maakt tegen kanker, een ziekte die op zichzelf al sterk beïnvloed is door ontregeling van lipidevlotten , wat op zijn beurt kan verklaren waarom kanker meer voorkomt bij ME.
De meest ‘diagnostische’ metabolieten:
Van alle metabolische reactiepaden die gemeten werden door Naviauxs team waren de volgende het vaakst onregelmatig in mannelijke en vrouwelijke testpersonen:
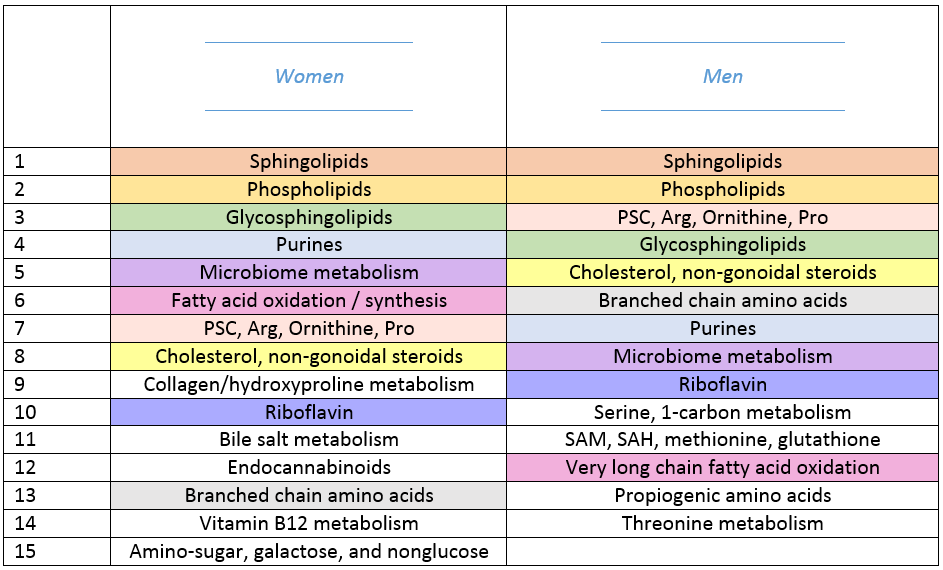
Lijst: De vaakst ontregelde metabolische subgroep bij vrouwen en mannen met ME/cvs
In het algemeen genomen waren deze patronen tegenovergesteld aan de patronen die we zien bij acute ontsteking en infectie: in plaats van een verpletterend, uitgerokken gevecht lijken de cellen zich neer te schurken in een poging om zo weinig mogelijk metabolisch ‘geluid’ te maken. Naviauxs team merkte op dat het patroon bij ME-patiënten bijna precies tegenovergesteld was aan hetgeen men ziet in systemische ontstekingsziektes zoals metabolisch syndroom en hartziekte.
Bovendien ontdekte Naviauxs team dat de analyse van verschillende van deze metabolieten diagnostisch kon zijn, in zulke mate dat zelfs één metaboliet een voorspeller van ziekte kon zijn; maar Naviauxs team merkte toch dat hun kleine testgroep uit de plaatselijke bevolking een unieke metabolietentest onrealistisch maakt, en raadt een onderzoek aan van 8 metabolieten voor mannen en 13 voor vrouwen, om een correcte diagnose te stellen.
Uiteindelijk vond Naviauxs team dat de opgetekende metabolische afwijkingen in direct verband stonden tot redox of de aanwezigheid van NADPH, een hoogenergetische molecule die nodig is om reacties van cellulaire ademhaling te voeden, dat uitgeput bleek bij patiënten.
Gevolgen:
Onder voorbehoud van replicatie van Naviauxs werk, en als zijn interpretaties kloppen, zullen de bevindingen enorme gevolgen hebben.
- We hebben een redelijke reeks biomarkers waaruit een werkbare diagnostische test kan komen.
- We kunnen beter begrijpen waarom ME geassocieerd is met ziektes zoals kanker en auto-immuniteit
- We kunnen beter begrijpen waarom een chemotherapeutisch middel als Rituximab de symptomen van ME kan verlichten.
- We hebben misschien een verklaring voor de ‘ziek maar nooit ziek’-toestand die veel patiënten ervaren: in cellen die overmatig gebruik maken van lipidevlotten om infectie te voorkomen ‘kent’ slechts een select groepje pathogenen hoe ze toch de cel binnen kunnen raken, en hypometabolische veranderingen zorgen als gevolg daarvan voor minder ‘voedsel’ (metabolieten die pathogenen graag lusten), wat verder de rem zet op de groei van pathogenen die geen voorkeur hebben voor door lipidevlotten ondersteunde infectie.
- Het verborgen houden van hulpbronnen en hypometabolisme kan verklaren waarom patiënten zo diepgaand vermoeid zijn , en kan een verklaring zijn voor PEM: er zijn simpelweg geen hulpbronnen.
- Uiteindelijk kunnen fouten in de opmaak of het metabolisme van lipidevlotten een diepgaand effect hebben op de biologie van elk systeem, aangezien lipidevlotten onrechtstreeks betrokken zijn bij celherkenning (fouten zouden auto-immuniteit veroorzaken), andere soorten celsignalering waaronder neuronale signalering, en zowel algemene immuunfunctie als de fysieke celintegriteit.
Wat we nog niet begrijpen, is tot welke potentiële behandelingsmogelijkheden dit zal leiden. Als deze ‘hibernatietoestand’ – die Naviaux ‘dauer’ noemt – een verdedigingsreactie is, dan is het misschien niet in ons voordeel om hem ‘uit te schakelen’, zeker als de aanvankelijke uitlokkende factor nog aanwezig is. We blijven geconfronteerd met één van de grootste en meest hardnekkige vraagstukken in ME-onderzoek: is de aanvankelijke uitlokkende pathogeen/stressor nog aanwezig of niet?
Patiënten die symptoomverlichting ervaren door schimmelwerende middelen, antibiotica of antivirale middelen, tonen in dit geval niet noodzakelijk aan dat er een actieve infectie is. Sommige antimicrobiële middelen doen lipidevlotten uiteenvallen, en zijn niet zo kieskeurig in hun aanval op pathogenen als we zouden denken. Om die reden duidt de doeltreffendheid van antimicrobiële behandelingen bij ME-patiënten niet noodzakelijk op de aanwezigheid van een op dit moment actieve infectie.
Spijtig genoeg is er misschien geen simpel ja/nee-antwoord. De aan- of afwezigheid van een systemische pathogeen zou ons kunnen leiden tot patiënt-subgroepen, met een patiëntengroep die nog een actieve of latente infectie heeft, en een andere die vastzit in een auto-immuunachtig symptoomplaatje waarbij het aanvankelijk uitlokkende pathogeen niet langer actief is, maar het systeem niet in staat is om los te komen uit de beschermende hibernatiemodus.
Er zijn nog steeds vele vragen te beantwoorden, en replicatiestudies te schrijven; maar toch is dit misschien wel het meest veelbelovende onderzoek naar ME sinds de mijlpaalstudie van Lipkin en Hornig over cytokines, met echte, positieve gevolgen voor de ME-gemeenschap.
- De paper van Naviaux et al. en de vraag-en-antwoordsessie vind je hier.
- Het bijkomend materiaal [niet vertaald, n.v.d.r.] vind je hier.
Opmerking: De paper die door Dr Naviaux en zijn onderzoeksteam geschreven werd, spreekt voorzichtiger over de gevolgen van de studie. Daarom wil ik een duidelijk onderscheid maken tussen mijn eigen veronderstellingen en die van Naviauxs paper:
Het is mijn hypothese dat metabolisme van lipidevlotten betrokken is bij het mechanisme waarlangs Rituximab symptomen bij ME-patiënten verlicht.
Het is mijn hypothese dat het uiteenvallen van lipidevlotten ervoor zorgt dat antimicrobiële middelen ME doeltreffend kunnen behandelen, zelfs als er geen pathogeen aanwezig is.
Hoewel het niet mijn hypothese is dat aggregatie van lipidevlotten een voordeel kan creëren voor bepaalde pathogenen boven andere, is het mijn hypothese dat het dat is wat ervoor zorgt dat bepaalde infecties vaker voorkomen bij ME-patiënten.
Het is mijn hypothese dat de ontregeling van lipidevlotten sommige pathogenen kan bevoordelen, terwijl het anderen afremt, wat uitmondt in een symptoomplaatje van patiënten die ‘ziek maar nooit ziek’ zijn.
Het is mijn hypothese dat ontregeling van lipidevlotten de overeenkomstige factor is tussen ME en kanker, wat te maken zou kunnen hebben met hun verhoogde coïncidentie.
© The Myalgic Encephalomyelitis Action Network. Vertaling Abby, redactie Zuiderzon, ME-gids.
Lees ook
- Onderzoekers identificeren kenmerkende chemische handtekening voor ME/cvs (Update)
- Het kernprobleem van ME/CVS geïdentificeerd? Naviauxs studie naar het metaboloom opent een nieuwe deur





